题目内容
14.下列说法正确的是( )| A. | Na2O2可作为潜艇工作人员的供氧剂 | |
| B. | 电解熔融NaCl可制得Na单质 | |
| C. | Fe3O4通常作为油漆原料 | |
| D. | 可用Ba(OH)2溶液区别NaHCO3溶液和Na2CO3溶液 |
分析 A、过氧化钠和二氧化碳、水蒸气反应生成氧气;
B、工业上电解熔融氯化钠得到氯气和钠;
C、氧化铁做油漆材料,四氧化三铁是磁铁;
D、氢氧化钡和碳酸钠、碳酸氢钠都发生反应生成白色沉淀.
解答 解:A、过氧化钠和二氧化碳、水蒸气反应生成氧气,Na2O2可作为潜艇工作人员的供氧剂,故A正确;
B、工业上电解熔融氯化钠得到氯气和钠,2NaCl$\frac{\underline{\;通电\;}}{\;}$2Na+Cl2↑,故B正确;
C、氧化铁做油漆材料,四氧化三铁是磁铁,是黑色固体,故C错误;
D、氢氧化钡和碳酸钠、碳酸氢钠都发生反应生成白色沉淀碳酸钡,不能鉴别碳酸钠和碳酸氢钠,故D错误;
故选AB.
点评 本题考查了物质性质的分析和应用,注意氧化铁的应用和碳酸钠、碳酸氢钠和氢氧化钡的反应理解,掌握基础是关键,题目较简单.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
9.据法国《科学与未来》杂志报道,美国科学家最近在实验室中合成了与脱氧核糖核酸(DNA)分子结构相近的苏糖核酸分子.一些专家认为这种物质包含遗传信息,可能是第三种遗传分子.苏糖核酸简称TNA,是DNA和RNA的“近亲”.TNA中含有苏糖的结构单元.已知苏糖的结构简式为:CH2OHCHOHCHOHCHO,以下有关苏糖的说法中不正确的是( )
| A. | 苏糖能发生银镜反应 | |
| B. | 苏糖与甲酸甲酯含碳的质量分数相同 | |
| C. | 苏糖在一定条件下能发生取代反应 | |
| D. | 苏糖与葡萄糖互为同分异构体 |
19.下列各溶液中,离子的物质的量浓度关系正确的是( )
| A. | pH=3的H2SO4溶液中:c(H+)=10-3mol•L-1 | |
| B. | 呈中性的醋酸和醋酸钠的混合溶液中:c(Na+)>c(CH3COO-) | |
| C. | 在Na2CO3溶液中,2c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) | |
| D. | 氯化铵溶液中:c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
6.下列因果关系叙述正确的是( )
| A. | Fe3+有氧化性,实验室常用KSCN溶液检验Fe3+ | |
| B. | SO2有较强的还原性,SO2可使酸性KMnO4溶液褪色 | |
| C. | Mg有还原性,电解MgCl2饱和溶液可制备Mg | |
| D. | 浓H2SO4有吸水性,浓H2SO4可使蔗糖炭化 |
 Ⅰ.在某温度时按n(N2):n(H2)=1:3的比例将混合气体投入密闭容器中反应:N2(g)+3H2(g)═2NH3(g)△H<0;
Ⅰ.在某温度时按n(N2):n(H2)=1:3的比例将混合气体投入密闭容器中反应:N2(g)+3H2(g)═2NH3(g)△H<0;

 ;E
;E .
. .
. .
.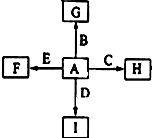 如图中,A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物,已知:①反应C+G$\stackrel{高温}{→}$B+H能放出大量的热,G为红棕色;②I是一种常见的温室气体,它和E可以发生反应:2E+I$\frac{\underline{\;点燃\;}}{\;}$ 2F+D,F中的E元素的质量分数为60%.回答问题:
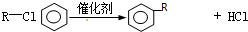
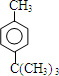
如图中,A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物,已知:①反应C+G$\stackrel{高温}{→}$B+H能放出大量的热,G为红棕色;②I是一种常见的温室气体,它和E可以发生反应:2E+I$\frac{\underline{\;点燃\;}}{\;}$ 2F+D,F中的E元素的质量分数为60%.回答问题: 丙二烯(H2C=C=CH2)是重要的基础有机化学原料,可由 FeCl3 催化格氏试剂与甲基丁炔氯制备.
丙二烯(H2C=C=CH2)是重要的基础有机化学原料,可由 FeCl3 催化格氏试剂与甲基丁炔氯制备.