题目内容
6.向一定量的饱和石灰水中不断通入二氧化碳,其溶液质量变化是( )| A. | 变小 | B. | 变大 | C. | 先变大后变小 | D. | 先变小后变大 |
分析 向一定量的石灰水中不断通入二氧化碳气体,开始二氧化碳与氢氧化钙反应生成碳酸钙沉淀,沉淀量不断增加,当氢氧化钙完全反应后继续通入二氧化碳,二氧化碳与碳酸钙和水反应生成易溶于水的碳酸氢钙,沉淀量不断减少,据此分析溶液质量变化.
解答 解:由题意知,随着不断通入CO2发生的化学反应为:Ca(OH)2+CO2═CaCO3↓+H2O,碳酸钙是沉淀,溶液质量减少,
当完全沉淀后继续通入二氧化碳时发生的反应CaCO3+H2O+CO2═Ca(HCO3)2,生成的碳酸氢钙是可溶性的强电解质,溶液质量变大,所以向一定量的饱和石灰水中不断通入二氧化碳,其溶液质量变化先变小后变大,
故选D.
点评 本题考查了溶液质量变化,明确开始二氧化碳与氢氧化钙反应生成碳酸钙沉淀,当氢氧化钙完全反应后继续通入二氧化碳,二氧化碳与碳酸钙和水反应生成易溶于水的碳酸氢钙的反应过程为解答关键,题目难度不大.

练习册系列答案
相关题目
11.高温下的反应SiO2+3C═SiC+2CO↑中,氧化剂和还原剂的质量比为( )
| A. | 1:2 | B. | 2:1 | C. | 1:3 | D. | 5:3 |
18.利用电化学原理保护钢闸门的某装置如图所示,关于该装置的说法正确的是( )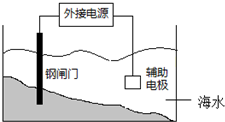

| A. | 钢闸门应与外接电源的负极相连 | |
| B. | 该装置的原理是“牺牲阳极阴极保护法” | |
| C. | 辅助电极材料可用锌 | |
| D. | 阴极的电极反应式:2Cl--2e→Cl2↑ |
15.下列关系的表述中正确的是( )
| A. | 向NaHSO3溶液中通入NH3至中性,溶液中存在:c(NH4+)>c(SO32-) | |
| B. | NH4Cl和NH3•H2O混合液pH=7,一定存在:c(NH4+)>c(Cl-) | |
| C. | NAHCO3溶液中存在HCO3-+H2O═H3O++CO32-,加水稀释后c(H+)减小 | |
| D. | pH相同的氯化铵与硫酸亚铁铵两种溶液中铵根离子浓度前者大 |
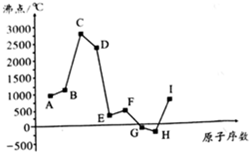 如图是周期表中原子序数小于20的某些元素的单质的沸点与原子序数的关系,图中的原子序数是连续的.
如图是周期表中原子序数小于20的某些元素的单质的沸点与原子序数的关系,图中的原子序数是连续的.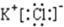 (写电子式).
(写电子式).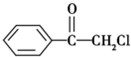 (1)苯氯乙酮是一具有荷花香味且有强催泪作用的化学试剂,它的结构简式如图 所示:则苯氯乙酮不可能具有的化学性质是ABD(填字母序号)
(1)苯氯乙酮是一具有荷花香味且有强催泪作用的化学试剂,它的结构简式如图 所示:则苯氯乙酮不可能具有的化学性质是ABD(填字母序号)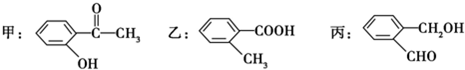
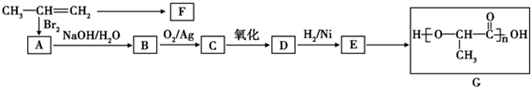
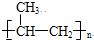 ;
; ;
;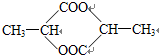 .
.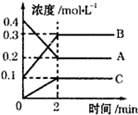 如图所示,800℃时A、B、C三种气体在密闭容器中反应时的浓度变化,分析图象,回答问题:
如图所示,800℃时A、B、C三种气体在密闭容器中反应时的浓度变化,分析图象,回答问题: 2B+C.
2B+C.