题目内容
18.利用电化学原理保护钢闸门的某装置如图所示,关于该装置的说法正确的是( )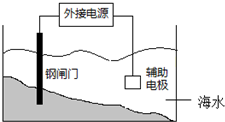
| A. | 钢闸门应与外接电源的负极相连 | |
| B. | 该装置的原理是“牺牲阳极阴极保护法” | |
| C. | 辅助电极材料可用锌 | |
| D. | 阴极的电极反应式:2Cl--2e→Cl2↑ |
分析 根据图示可知,此电化学防护的方法为外加电源的阴极保护法,即钢闸门、辅助电极和外接电源构成电解池,其中钢闸门做电解池的阴极被保护,辅助电极做阳极,据此分析.
解答 解:根据图示可知,此电化学防护的方法为外加电源的阴极保护法,即钢闸门、辅助电极和外接电源构成电解池,其中钢闸门做电解池的阴极被保护,辅助电极做阳极.
A、钢闸门做阴极,故应与外接电源的负极相连,故A正确;
B、该装置的原理是外加电源的阴极保护法,故B错误;
C、辅助电极材料做阳极,如果用锌,则锌会被消耗,故从节约能源的角度来看,应用惰性电极更合适,故C错误;
D、阴极上是电解质溶液中的阳离子放电,故电极反应为:2H2O+2e-=H2+2OH-,故D错误.
故选A.
点评 本题考查了金属的电化学腐蚀和防护,应注意的是牺牲阳极的阴极保护法是原电池原理,外加电源的阴极保护法为电解池原理.

练习册系列答案
相关题目
8.现有8种元素的性质、数据如表所列,它们属于第二或第三周期.
回答下列问题:
(1)①在元素周期表中的位置是第二周期VIA.写出②最高价氧化物对应水化物跟⑤的氢化物水溶液反应的离子方程式:Mg(OH)2+2H+=Mg2++2H2O.
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是HClO4;碱性最强的化合物属于离子化合物(填“离子”或“共价”).
(3)比较④和⑦的氢化物的稳定性(用化学式表示)NH3>PH3.
| ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |
| 原子半径(10-10m) | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 | 0.82 |
| 最高或最低化合价 | +2 | +1 | +5 | +7 | +1 | +5 | +3 | |
| -2 | -3 | -1 | -3 |
(1)①在元素周期表中的位置是第二周期VIA.写出②最高价氧化物对应水化物跟⑤的氢化物水溶液反应的离子方程式:Mg(OH)2+2H+=Mg2++2H2O.
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是HClO4;碱性最强的化合物属于离子化合物(填“离子”或“共价”).
(3)比较④和⑦的氢化物的稳定性(用化学式表示)NH3>PH3.
6.向一定量的饱和石灰水中不断通入二氧化碳,其溶液质量变化是( )
| A. | 变小 | B. | 变大 | C. | 先变大后变小 | D. | 先变小后变大 |
13.生活中处处有化学.下列相关表述正确的是( )
| A. | 天然橡胶的主要成分是异戊二烯 | |
| B. | 通过物理变化将煤气化和液化,能高效清洁地用煤 | |
| C. | 苯酚能用于环境消毒 | |
| D. | 乙醇是不可再生的能源 |
3.β-月桂烯的结构如图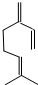 所示,一分子该物质与溴发生加成反应,得到的产物(只考虑位置异构)理论上最多有( )
所示,一分子该物质与溴发生加成反应,得到的产物(只考虑位置异构)理论上最多有( )
 所示,一分子该物质与溴发生加成反应,得到的产物(只考虑位置异构)理论上最多有( )
所示,一分子该物质与溴发生加成反应,得到的产物(只考虑位置异构)理论上最多有( )| A. | 6种 | B. | 7种 | C. | 8种 | D. | 9种 |
10.现代生活需要人们有一定的科学素养,下列有关化学的科学常识正确的是( )
| A. | 利用SiO2的导电性来制备光导纤维 | |
| B. | 可用热的饱和碳酸钠溶液除去金属表面的矿物油 | |
| C. | “地沟油”不能食用,但可以加工成肥皂或生物柴油 | |
| D. | 发展新能源汽车的主要目的是为了减少PM2.5的排放 |
8.向200mL 0.1mol/L 的Fe(NO3)2溶液中加入一定量NaOH,使Fe2+完全沉淀,过滤、加热并灼烧直至质量不再变化,此时固体的质量可能为( )
| A. | 1.60 g | B. | 2.76 g | C. | 4.36 g | D. | 5.54 g |
 X、Y、Z、Q、R为原子序数依次增大的前四周期元素.X的一种1﹕2型氢化物分子中既有σ键又有π键,且分子中所有原子共平面;Z的L层有2个未成对电子;Q是所在周期中电负性最大的元素,QZ2可替代Q2作新的自来水消毒剂;R在周期表中位于d区,其基态原子有两个能级处于半充满状态.
X、Y、Z、Q、R为原子序数依次增大的前四周期元素.X的一种1﹕2型氢化物分子中既有σ键又有π键,且分子中所有原子共平面;Z的L层有2个未成对电子;Q是所在周期中电负性最大的元素,QZ2可替代Q2作新的自来水消毒剂;R在周期表中位于d区,其基态原子有两个能级处于半充满状态.