题目内容
9.下列溶液中物质的量浓度为1mol•L-1的是( )| A. | 将20gNaOH溶解在500mL水中 | |
| B. | 将22.4L HCl气体溶于水配成1 L溶液 | |
| C. | 将1 L 10 mol•L-1浓盐酸加入9L水中 | |
| D. | 将10gNaOH溶解在少量水中,恢复至室温,再加蒸馏水直到溶液体积为250mL |
分析 结合n=$\frac{m}{M}$、n=$\frac{V}{Vm}$、c=$\frac{n}{V}$计算.
解答 解:A.500mL水为溶剂的体积,溶液体积未知,不能计算浓度,故A不选;
B.状况未知,Vm不确定,不能利用体积计算,故B不选;
C.加入9L水中,溶液的体积不是10L,故C不选;
D.将10gNaOH溶解在少量水中,恢复至室温,再加蒸馏水直到溶液体积为250mL,则NaOH的浓度为$\frac{\frac{10g}{40g/mol}}{0.25L}$=1mol/L,故D选;
故选D.
点评 本题考查物质的量浓度的计算,为高频考点,把握质量、体积、物质的量的关系为解答的关键,侧重分析与计算能力的考查,注意状况及溶液体积的判断,题目难度不大.

练习册系列答案
相关题目
19.通常人们把拆开1mol某化学键所吸收的能量看成该化学键的键能.现给出化学键的键能(见表):
请计算N2(g)+3H2(g)═2NH3(g)的反应热( )
| 化学键 | H-H | N三N | N-H |
| 键能/(kJ•mol-1) | 436 | 945.6 | 391 |
| A. | +192.4 kJ•mol-1 | B. | +92.4kJ•mol-1 | C. | -92.4kJ•mol-1 | D. | -192.4kJ•mol-1 |
4.甲、乙、丙、丁四种物质中,甲、乙、丙均含有相同的某种元素,它们之间具有如下转化关系甲$\stackrel{丁}{→}$乙$?_{甲}^{丁}$丙,下列有关物质的推断不正确的是( )
| A. | 若甲为焦炭,则丁可能是O2 | B. | 若甲为AlCl3,则丁可能是浓氨水 | ||
| C. | 若甲为SO2,则丁可能是氨水 | D. | 若甲为NaOH 溶液,则丁可能是H2S |
14.可以用于鉴别淀粉溶液和蛋白质溶液的方法是( )
| A. | 分别加入碘化钾溶液,观察颜色变化 | |
| B. | 分别加热,观察是否生成沉淀 | |
| C. | 分别滴加浓硝酸 | |
| D. | 分别灼烧,闻味道 |
1.已知反应:①101kPa时,2C(s)+O2(g)═2CO(g)△H1=-221kJ/mol
②稀溶液中,H+(aq)+OH-(aq)═H2O(l)△H2=-57.3kJ/mol.
下列结论正确的是( )
②稀溶液中,H+(aq)+OH-(aq)═H2O(l)△H2=-57.3kJ/mol.
下列结论正确的是( )
| A. | 碳的燃烧热为221KJ/mol | |
| B. | 稀盐酸与稀NaOH溶液反应生成1mol水,放出的热量57.3KJ | |
| C. | 浓硫酸与稀NaOH溶液反应的中和热值为57.3KJ/mol | |
| D. | 稀醋酸与稀NaOH溶液反应生成1mol水,放出的热量57.3KJ |
18.下列不属于自发进行的变化是( )
| A. | 红墨水加到清水使整杯水变红 | B. | 冰在室温下融化成水 | ||
| C. | 水电解生成氢气和氧气 | D. | 铁器在潮湿的空气中生锈 |
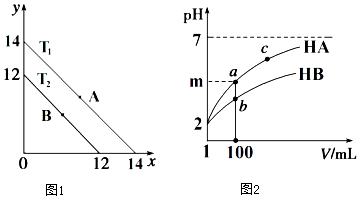 (1)溶液中,c(H+)=10-x mol•L-1,c(OH-)=10-y mol•L-1,x与y的关系如图1所示.
(1)溶液中,c(H+)=10-x mol•L-1,c(OH-)=10-y mol•L-1,x与y的关系如图1所示.