题目内容
1.已知反应:①101kPa时,2C(s)+O2(g)═2CO(g)△H1=-221kJ/mol②稀溶液中,H+(aq)+OH-(aq)═H2O(l)△H2=-57.3kJ/mol.
下列结论正确的是( )
| A. | 碳的燃烧热为221KJ/mol | |
| B. | 稀盐酸与稀NaOH溶液反应生成1mol水,放出的热量57.3KJ | |
| C. | 浓硫酸与稀NaOH溶液反应的中和热值为57.3KJ/mol | |
| D. | 稀醋酸与稀NaOH溶液反应生成1mol水,放出的热量57.3KJ |
分析 A.燃烧热中C应生成稳定氧化物为二氧化碳;
B.稀的强酸与强碱反应生成1mol水放出的热量为中和热;
C.浓硫酸溶于水放出大量的热;
D.醋酸电离吸收热量.
解答 解:A.燃烧热中C应生成稳定氧化物为二氧化碳,则碳的燃烧热中热量应大于为221KJ,故A错误;
B.稀的强酸与强碱反应生成1mol水放出的热量为中和热,则稀盐酸与稀NaOH溶液反应生成1mol水,放出的热量57.3KJ,故B正确;
C.浓硫酸溶于水放出大量的热,则浓硫酸与稀NaOH溶液反应的中和热数值大于57.3KJ/mol,故C错误;
D.醋酸电离吸收热量,则稀醋酸与稀NaOH溶液反应生成1mol水,放出的热量小于57.3KJ,故D错误;
故选B.
点评 本题考查反应热与焓变,为高频考点,把握中和热、燃烧热及能量变化为解答的关键,侧重分析与应用能力的考查,注意溶解、电离中的热效应,题目难度不大.

练习册系列答案
相关题目
9.下列溶液中物质的量浓度为1mol•L-1的是( )
| A. | 将20gNaOH溶解在500mL水中 | |
| B. | 将22.4L HCl气体溶于水配成1 L溶液 | |
| C. | 将1 L 10 mol•L-1浓盐酸加入9L水中 | |
| D. | 将10gNaOH溶解在少量水中,恢复至室温,再加蒸馏水直到溶液体积为250mL |
16.下列选项中能表示阿伏加德罗常数数值的是( )
| A. | 1mol H+含有的电子数 | |
| B. | 标准状况下,22.4L酒精所含的分子数 | |
| C. | 1.6 g CH4 含有的质子数 | |
| D. | 1L 1mol/L的硫酸钠溶液所含的Na+ 数 |
6.与30mL 1mol/LAlCl3溶液中c(Cl-)相等的是( )
| A. | 50mL 3mol/L的KCl溶液 | B. | 30mL 1mol/L的NaCl溶液 | ||
| C. | 30mL 3mol/L的FeCl3溶液 | D. | 10mL3mol/L的AlCl3溶液 |
13.下列各组离子中,在酸性溶液中能大量共存且溶液为无色透明的是( )
| A. | Na+、Cu2+、Cl-、SO42- | B. | Na+、HCO3-、Cl-、NO3- | ||
| C. | Na+、SO32-、NO3-、K+ | D. | K+、SO42-、Mg2+、Cl- |
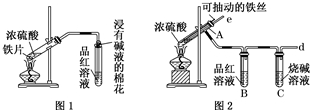 某校化学兴趣小组为探究铁与浓硫酸反应,设计了图1、图2所示装置进行实验.
某校化学兴趣小组为探究铁与浓硫酸反应,设计了图1、图2所示装置进行实验.