��Ŀ����
1������������ԭΪ���ļ��������������Ľ�����ռ��ʮ����Ҫ�ĵ�λ��������¯�з����Ĺؼ���Ӧ���£�C��s��+O2��g���TCO2��g����H=-393.5kJ/mo1
CO2��g��+C��s���T2CO��g����H=+172.46kJ/mo1
Fe2O3+CO��Fe+CO2
����֪��$2Fe��s��+\frac{3}{2}{O_2}��g���TF{e_2}{O_3}��S����H=-824.21kJ/mo1$
�������������Ȼ�ѧ��Ӧ����ʽ���ش��������⣺
��1��CO��ȼ����Ϊ282.98KJ/mol��д�����Ȼ�ѧ��Ӧ����ʽCO��g��+$\frac{1}{2}$O2��g��=CO2��g����H=-282.98KJ/mol��
��2����¯��Fe2O3��CO��ԭΪFe���Ȼ�ѧ��Ӧ����ʽΪFe2O3��s��+3CO��g��=2Fe��s��+3CO2��g����H=-24.74kJ•mol-1��
��3������1t����96%���������轹̿������������0.31t����������λ��Ч���֣�
���� ��1��ȼ������1mol��ȼ����ȫȼ�������ȶ�������ų�������������Ȼ�ѧ����ʽ��˹���ɼ���õ���
��2����C��s��+O2��g���TCO2��g����H=-393.5kJ•mol-1
��CO2��g��+C��s���T2CO��g����H=172.46kJ•mol-1
��2Fe��s��+$\frac{3}{2}$O2��g���TFe2O3��s����H=-824.21kJ•mol-1
����ݸ�˹���ɢ١�$\frac{3}{2}$-�ڡ�$\frac{3}{2}$-�۽��з������㣻
��3�����������ķ���ʽ2C+O2$\frac{\underline{\;��ȼ\;}}{\;}$2CO��Fe2O3+3CO$\frac{\underline{\;����\;}}{\;}$2Fe+3CO2���м��㣮
��� �⣺��1����C��s��+O2��g��=CO2��g����H=-393.5 kJ•mol-1
��CO2��g��+C��s��=2CO��g����H=172.46 kJ•mol-1
���ݸ�˹���ɼ����-�ڵõ���2CO��g��+O2��g��=2CO2��g����H=-565.96KJ/mol��
����ȼ���ȸ����֪��һ����̼ȼ����Ϊ282.98KJ/mol���Ȼ�ѧ����ʽΪ��CO��g��+$\frac{1}{2}$O2��g��=CO2��g����H=-282.98KJ/mol��
�ʴ�Ϊ��282.98KJ/mol��CO��g��+$\frac{1}{2}$O2��g��=CO2��g����H=-282.98KJ/mol��
��2����C��s��+O2��g���TCO2��g����H=-393.5kJ•mol-1
��CO2��g��+C��s���T2CO��g����H=172.46kJ•mol-1
��2Fe��s��+$\frac{3}{2}$O2��g���TFe2O3��s����H=-824.21kJ•mol-1
����ݸ�˹���ɢ١�$\frac{3}{2}$-�ڡ�$\frac{3}{2}$--�ۣ���Fe2O3��s��+3CO��g��=2Fe��s��+3CO2��g����H=-393.5��$\frac{3}{2}$-172.46��$\frac{3}{2}$+824.2=-24.74kJ•mol-1��
�ʴ�Ϊ��Fe2O3��s��+3CO��g��=2Fe��s��+3CO2��g����H=-24.74kJ•mol-1��
��3����CO����Ϊx
Fe2O3+3CO$\frac{\underline{\;����\;}}{\;}$2Fe+3CO2
84 112
x 0.96t
x=0.72t
��C������Ϊy
2C+O2$\frac{\underline{\;����\;}}{\;}$2CO
24 56
y 0.72t
y=0.31t
�ʴ�Ϊ��0.31t��
���� ���⿼���˹���ɵ�Ӧ���Լ���ѧ����ʽ���йؼ��㣬��ȷӦ�ø�˹�����ǽⱾ��ؼ�����Ŀ�ѶȲ���

| A�� | 10g H2 ��10g O2 | B�� | 5.6L N2����״���£���11gCO2 | ||
| C�� | 9��H2O��11.2L O2 | D�� | 224mL H2����״���£���0.1mol��N2 |
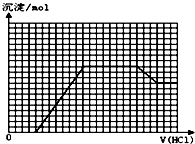 ij��ɫ��ҺM���ܺ�������OH-��HCO3-��CO32-��SO42-��SiO32-��AlO2-��NH4+��MnO4-��Cu2+��Mg2+��Na+��Fe3+�е������֣�ȡһ������M��Һ�μ����ᣬ�������������ʵ�������������Ĺ�ϵ��ͼ��ʾ��HCO3-��Al3+��AlO2-��Ҫ��Ӧ�������棩�������ж���ȷ���ǣ�������
ij��ɫ��ҺM���ܺ�������OH-��HCO3-��CO32-��SO42-��SiO32-��AlO2-��NH4+��MnO4-��Cu2+��Mg2+��Na+��Fe3+�е������֣�ȡһ������M��Һ�μ����ᣬ�������������ʵ�������������Ĺ�ϵ��ͼ��ʾ��HCO3-��Al3+��AlO2-��Ҫ��Ӧ�������棩�������ж���ȷ���ǣ�������| A�� | ԭ��Һ�п��ܺ���NH4+��SO42- | |
| B�� | ������Һ�����ٺ�2������ | |
| C�� | ԭ��Һ��n��NaAlO2����n��Na2CO3��=1��1 | |
| D�� | �μ������ʼ�η�����Ӧ�����ӷ���ʽ�ǣ�CO32-+H+�THCO3- |
| 1 | A | |||||||||||||||||
| 2 | B | |||||||||||||||||
| 3 | C | D | E | F | G | H | I | |||||||||||
| 4 | J | K | ||||||||||||||||
| 5 | ||||||||||||||||||
| 6 | ||||||||||||||||||
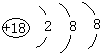 ��
����2����������ĸ�����Ԫ���У����γ��������������Ԫ����Al ����Ԫ�ط��ű�ʾ����д����Ԫ�صĵ�����C����������ˮ���ﷴӦ�Ļ�ѧ����ʽ2Al+2NaOH+2H2O=2NaAlO2+3H2����
��3����C��D��E�γɵ����������У�������ǿ����NaOH���û�ѧʽ��ʾ������F��G��H�γɵ��⻯�������ȶ�����HCl���û�ѧʽ��ʾ����
��4��A��B���γ�����л��������ṹʽΪ
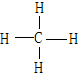 �����Ŀռ乹�����������壮
�����Ŀռ乹�����������壮��5����H��K��Ӧ�ĵ����У������Խ�������Br2���û�ѧʽ��ʾ����
��6��JԪ���ǹ���Ԫ��������ҵ�ϳ��ó�������Ҫ�ɷ�ΪFe2O3��Ϊԭ�ϣ����ø�¯�����ķ�ʽ��������ԭ���ǣ��ѳ�����̼��ʯ��ʯһ������¯���ڸ����£������ӳ������л�ԭ������д���÷�Ӧ�Ļ�ѧ����ʽFe2O3+3CO$\frac{\underline{\;����\;}}{\;}$2Fe+3CO2��
 ��������ˮ�����г�����ɱ��������HClO��ɱ��������ClO-ǿ��25��ʱ����-��ˮ��ϵ�д�������ƽ���ϵ��
��������ˮ�����г�����ɱ��������HClO��ɱ��������ClO-ǿ��25��ʱ����-��ˮ��ϵ�д�������ƽ���ϵ����Cl2��g��?Cl2��aq����K1=10-1.2
��Cl2��aq��+H2O?HClO+H++Cl-��K2=10-3.4
��HClO?H++ClO-��Ka=��
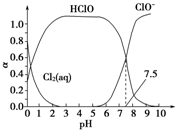
����Cl2��aq����HClO��ClO-�ֱ�����������ռ������������pH�仯�Ĺ�ϵ��ͼ��ʾ�����б�������ȷ���ǣ�������
| A�� | ��ͼ���֪��Ka=10-7.5 | |
| B�� | ���ȴ���ˮ��ϵ�У�c��HClO��+c��ClO-����c��H+��-c��OH-�� | |
| C�� | ���ȴ�������ˮʱ��ɱ��Ч�����pH��ΧΪ3��6 | |
| D�� | ������-��ˮ��ϵ�м�����̼��ƣ��������ϵƯ���� |
| A�� | C14H18O5 | B�� | C14H16O4 | C�� | C16H22O5 | D�� | C16H20O5 |
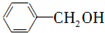
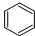 c��
c��
 ��������������һ������ĭ���еIJ��Ͼ۱���ϩ��
��������������һ������ĭ���еIJ��Ͼ۱���ϩ�� ��
�� ��
�� ���������£���������ʡ�ԣ�
���������£���������ʡ�ԣ�
 ��
�� ��
�� ��
�� ��
�� ��
��