题目内容
12.在一密闭容器中,放入镍粉并充入一定量的CO气体,一定条件下发生反应:Ni(s)+4CO(g)?Ni(CO)4(g),已知该反应在25℃和80℃时的平衡常数分别为5×104和2,下列说法正确的是( )
| A. | 上述生成Ni(CO)4(g)的反应为放热反应 | |
| B. | 在80℃时,测得某时刻,Ni(CO)4、CO浓度均为0.5 mol•L-1,则此时v(正)<v(逆) | |
| C. | 恒温恒压下,向容器中再充入少量的Ar,上述平衡将正向移动 | |
| D. | 恒温恒容下,向容器中再充入少量Ni(CO)4(g),达新平衡时,CO 的百分含量将增大 |
分析 A、依据平衡常数随温度变化分析判断平衡移动方向,结合平衡移动原理判断;
B、依据浓度商和平衡常数比较判断反应进行的方向;
C、恒温恒压下,向容器中再充入少量的Ar,平衡向气体体积增大的方向进行;
D、增大Ni(CO)4(g),相当于增大压强,平衡正向进行.
解答 解:A、平衡常数数据分析,平衡常数随温度升高减小,说明平衡逆向进行,逆向是吸热反应,正向是放热反应,故A正确;
B、80℃时,测得某时刻Ni(CO)4(g)、CO(g)浓度均为0.5 mol•L-1,Qc=$\frac{c(Ni(CO)_{4})}{{c}^{4}(CO)}$=$\frac{0.5}{0.{5}^{4}}$=8>2,说明平衡逆向进行,则此时v(正)<v(逆),故B正确;
C、恒温恒压下,向容器中再充入少量的Ar,压强增大保持恒压,平衡向气体体积增大的方向进行,上述平衡将逆向移动,故C错误;
D、恒温恒容下,向容器中再充入少量的Ni(CO)4(g),相当于增大压强平衡正向进行,达到新平衡时,CO的百分含量将减小,故D错误;
故选AB.
点评 本题考查了平衡常数的计算和数据判断应用,影响平衡因素分析,掌握基础是解题关键,题目难度中等.

练习册系列答案
 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案
相关题目
7.下列图示实验操作,能达到目的是( )
| A. |  检验K+的存在 | B. |  | C. |  蒸馏 蒸馏 | D. |  检查气密性 |
17.如图为反应2X(g)+Y(s)?2Z(g)的反应过程和能量关系图,下列说法正确的是( )

| A. | 曲线a和b表示两个反应过程的反应热不同 | |
| B. | 曲线a一定表示反应是在无催化剂时的反应过程 | |
| C. | 增大压强,X的转化率一定增大 | |
| D. | 反应达平衡,升高温度,平衡常数K值一定减小 |
4.(1)二氧化硫的催化氧化的过程如图1所示,

其中a、c二步的化学方程式可表示为:SO2+V2O5?SO3+V2O4 4VOSO4+O2?2V2O5+4SO3.该反应的催化剂是V2O5(写化学式)
(2)压强及温度对SO2转化率的影响如下表(原料气各成分的体积分数为:SO2 7%,O2 11%,N2 82%):
当合成SO3的反应达到平衡后,改变某一外界条件(不改变SO2、O2和SO3的量),反应速率与时间的关系如图2所示.图中t1时引起平衡移动的条件可能是增大压强其中表示平衡混合物中SO3的含量最高的一段时间是t2-t3.
(3)550℃时,SO2转化为SO3的平衡转化率(α)与体系总压强(p)的关系如右图3所示.将2.0mol SO2和1.0mol O2置于5 L密闭容器中,反应达平衡后,体系总压强为0.10M Pa.试计算反应2SO3?2SO2+O2 在550℃时的平衡常数K=2.5×10-3.
反应达平衡后,下列措施中能使n(SO3)/n(SO2)增大的是CD
A.升高温度 B.充入He(g),使体系总压强增大
C.再充入2mol SO2和1mol O2 D.再充入1mol SO2和1mol O2
(4)SO3溶于水得到硫酸.在25°C下,将x mol•L-1的氨水与y mol•L-1的硫酸等体积混合,反应后溶液中显中性,则c(NH4+)=2c(SO42-)(填“>”、“<”或“=”);用含x和y的代数式表示出氨水的电离平衡常数$\frac{2×1{0}^{-7}y}{x-2y}$.

其中a、c二步的化学方程式可表示为:SO2+V2O5?SO3+V2O4 4VOSO4+O2?2V2O5+4SO3.该反应的催化剂是V2O5(写化学式)
(2)压强及温度对SO2转化率的影响如下表(原料气各成分的体积分数为:SO2 7%,O2 11%,N2 82%):
| 压强/MPa 温度/℃ | 0.1 | 0.5 | 1 | 10 |
| 400 | 99.2% | 99.6% | 99.7% | 99.9% |
| 500 | 93.5% | 96.9% | 97.8% | 99.3% |
| 600 | 73.7% | 85.8% | 89.5% | 96.4% |
(3)550℃时,SO2转化为SO3的平衡转化率(α)与体系总压强(p)的关系如右图3所示.将2.0mol SO2和1.0mol O2置于5 L密闭容器中,反应达平衡后,体系总压强为0.10M Pa.试计算反应2SO3?2SO2+O2 在550℃时的平衡常数K=2.5×10-3.
反应达平衡后,下列措施中能使n(SO3)/n(SO2)增大的是CD
A.升高温度 B.充入He(g),使体系总压强增大
C.再充入2mol SO2和1mol O2 D.再充入1mol SO2和1mol O2
(4)SO3溶于水得到硫酸.在25°C下,将x mol•L-1的氨水与y mol•L-1的硫酸等体积混合,反应后溶液中显中性,则c(NH4+)=2c(SO42-)(填“>”、“<”或“=”);用含x和y的代数式表示出氨水的电离平衡常数$\frac{2×1{0}^{-7}y}{x-2y}$.
1.下列有关说法不正确的是( )
| A. | 25℃时,0.1mol•L-1的三种溶液的pH关系为:pH(Na2CO3)>pH(NaHCO3)>pH(CH3COONa) | |
| B. | 25℃时,pH=5的CH3COOH溶液和pH=5的NH4Cl溶液,c(H+)相等 | |
| C. | 25℃时,BaCO3在纯水中的KSP比在Na2CO3溶液中的KSP大 | |
| D. | NaHCO3和Na2CO3混合溶液中,一定有c(Na+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-) |
2.下列装置所示的实验中,能达到实验目的是( )
| A. | 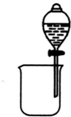 分离碘酒中的碘和酒精 | B. | 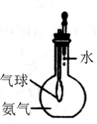 验证氨气易溶于水 | ||
| C. | 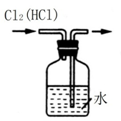 除去Cl2中的HCl杂质 | D. | 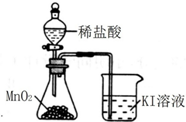 比较MnO2、Cl2、I2 |
 2O(g)=C2H5OH(g)的△H为( )
2O(g)=C2H5OH(g)的△H为( ) 2SO3 是工业上制造硫酸的重要反应。下列关于该反应的说法正确的是
2SO3 是工业上制造硫酸的重要反应。下列关于该反应的说法正确的是