题目内容
17.如图为反应2X(g)+Y(s)?2Z(g)的反应过程和能量关系图,下列说法正确的是( )
| A. | 曲线a和b表示两个反应过程的反应热不同 | |
| B. | 曲线a一定表示反应是在无催化剂时的反应过程 | |
| C. | 增大压强,X的转化率一定增大 | |
| D. | 反应达平衡,升高温度,平衡常数K值一定减小 |
分析 A.依据反应的焓变=反应物的总键能-生成物的总键能,△H=E1-E2;
B.依据正催化剂能降低反应活化能,而负催化剂能增大反应的活化能;
C.依据前后气体系数之和相等的可逆反应,增大压强平衡不移动;
D.依据图象分析,反应物能量高于于生成物,反应是放热反应,升高温度平衡向吸热的方向移动,平衡逆向移动,平衡常数K减小;
解答 解:A.反应的焓变=反应物的总键能-生成物的总键能,△H=E1-E2,b是加入催化剂,改变反应速率,不改变化学平衡,所以曲线a和b表示两个反应过程的反应热相同,故A错误;
B.正催化剂能降低反应活化能,而负催化剂能增大反应的活化能,所以曲线a不一定表示反应是在无催化剂时的反应过程,故B错误;
C.反应2X(g)+Y(s)?2Z(g)前后气体系数之和相等,增大压强平衡不移动,X的转化率不变,故C错误;
D.依据图象分析,反应物能量高于于生成物,反应是放热反应,升高温度平衡向吸热的方向移动,即逆向反应,平衡常数K值一定减小,故D正确;
故选D.
点评 本题考查了焓变的分析判断,图象分析是解题关键,理解含义注意知识的联系,题目较简单.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
12.在一密闭容器中,放入镍粉并充入一定量的CO气体,一定条件下发生反应:
Ni(s)+4CO(g)?Ni(CO)4(g),已知该反应在25℃和80℃时的平衡常数分别为5×104和2,下列说法正确的是( )
Ni(s)+4CO(g)?Ni(CO)4(g),已知该反应在25℃和80℃时的平衡常数分别为5×104和2,下列说法正确的是( )
| A. | 上述生成Ni(CO)4(g)的反应为放热反应 | |
| B. | 在80℃时,测得某时刻,Ni(CO)4、CO浓度均为0.5 mol•L-1,则此时v(正)<v(逆) | |
| C. | 恒温恒压下,向容器中再充入少量的Ar,上述平衡将正向移动 | |
| D. | 恒温恒容下,向容器中再充入少量Ni(CO)4(g),达新平衡时,CO 的百分含量将增大 |
9.下列说法中一定正确的是( )
| A. | pH=7的溶液呈中性 | |
| B. | pH值为0的溶液中c(H+)=0 mol/L | |
| C. | pH=5的溶液中[H+]=1.0×10-5 mol•L-1 | |
| D. | pH=5的溶液中[OH-]=1.0×10-9 mol•L-1 |
 H+(溶液)+In-(溶液,黄色) 而用作酸碱指示剂。往该溶液中加入Na2O2粉末,则溶液颜色为( )
H+(溶液)+In-(溶液,黄色) 而用作酸碱指示剂。往该溶液中加入Na2O2粉末,则溶液颜色为( )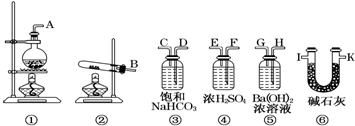
 某研究小组为探究SO2和Fe(NO3)3溶液的反应的实质.设计了如图所示装置进行实验.已知:1.0mol/L的Fe(NO3)3溶液的pH=1.
某研究小组为探究SO2和Fe(NO3)3溶液的反应的实质.设计了如图所示装置进行实验.已知:1.0mol/L的Fe(NO3)3溶液的pH=1.