题目内容
下列图示实验现象及其解释不正确的是( )
A、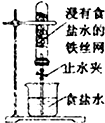 一段时间后打开止水夹,观察到导管中液面上升,因为铁发生了吸氧腐蚀 |
B、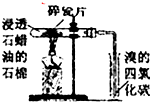 加热一段时间,观察到溴的四氯化碳溶液颜色褪去,因为有气态烯烃产生 |
C、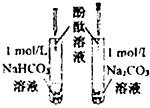 溶液均变红,碳酸钠溶液颜色较深,因为相同条件下水解能力HCO3-强于CO32- |
D、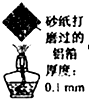 加热一段时间,观察到熔化的铝未滴落,因为铝表面生成氧化铝的熔点很高 |
考点:化学实验方案的评价
专题:实验评价题
分析:A.食盐水为中性溶液,发生吸氧腐蚀,氧气减少,液面上升;
B.加热石蜡油生成乙烯,乙烯与溴水发生加成反应;
C.均水解,且水解能力HCO3-小于CO32-;
D.氧化铝的熔点高,包裹在Al的外面,熔化的铝未滴落.
B.加热石蜡油生成乙烯,乙烯与溴水发生加成反应;
C.均水解,且水解能力HCO3-小于CO32-;
D.氧化铝的熔点高,包裹在Al的外面,熔化的铝未滴落.
解答:
解:A.食盐水为中性溶液,发生吸氧腐蚀,氧气减少,则一段时间后打开止水夹,观察到导管中液面上升,故A正确;
B.加热石蜡油生成乙烯,乙烯与溴水发生加成反应,则观察到溴的四氯化碳溶液颜色褪去,因为有气态烯烃产生,故B正确;
C.均水解,且水解能力HCO3-小于CO32-,则碳酸钠溶液颜色较深,故C错误;
D.氧化铝的熔点高,包裹在Al的外面,熔化的铝未滴落,则观察到熔化的铝未滴落,是因为铝表面生成氧化铝的熔点很高,故D正确;
故选C.
B.加热石蜡油生成乙烯,乙烯与溴水发生加成反应,则观察到溴的四氯化碳溶液颜色褪去,因为有气态烯烃产生,故B正确;
C.均水解,且水解能力HCO3-小于CO32-,则碳酸钠溶液颜色较深,故C错误;
D.氧化铝的熔点高,包裹在Al的外面,熔化的铝未滴落,则观察到熔化的铝未滴落,是因为铝表面生成氧化铝的熔点很高,故D正确;
故选C.
点评:本题考查化学实验方案的评价,为高频考点,涉及电化学腐蚀、乙烯的性质、盐类水解、氧化铝的性质等,把握物质的性质及化学反应原理为解答的关键,侧重化学反应原理的考查,注意图中装置及操作的可行性、评价性分析,题目难度不大.

练习册系列答案
相关题目
下列离子或分子组中大量共存且满足相应要求的是( )
| A、K+、AlO2-、Cl-、MnO4- 要求:无色澄清溶液 |
| B、Fe3+、NO3-、I-、HCO3- 要求:逐滴滴加盐酸立即产生气体 |
| C、Na+、K+、Ag+、NO3- 要求:逐滴滴加氨水先有沉淀产生,后沉淀消失 |
| D、NH4+、Al3+、SO42-、CH3COOH 要求:滴加NaOH浓溶液立刻产生气体 |
某反应的△H=+100kJ?mol-1,下列有关该反应的叙述正确的是( )
| A、正反应活化能不小于100kJ?mol-1 |
| B、正反应活化能小于100kJ?mol-1 |
| C、逆反应活化能一定小于100kJ?mol-1 |
| D、正反应活化能比逆反应活化能小100kJ?mol-1 |
某有机物的结构如图所示,下列有关它的说法正确的是( )


| A、能与氢氧化钠溶液反应 |
| B、4个碳原子可能在同一平面内 |
| C、与它具有相同官能团的同分异构体还有4种 |
| D、与乙醇互为同系物 |
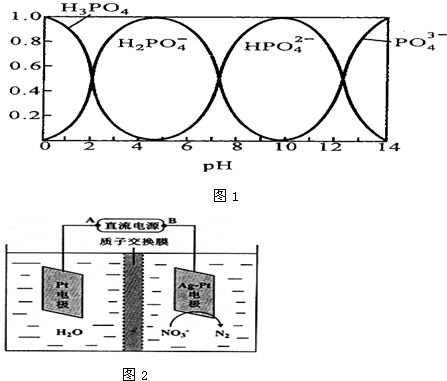
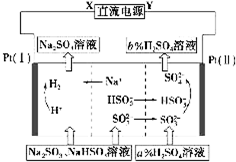 用Na2SO3溶液吸收硫酸工业尾气中的二氧化硫,将所得的混合液进行电解循环再生,这种新工艺叫再生循环脱硫法.其中阴、阳离子交换膜组合循环再生机理如图所示,则下列有关说法中正确的是( )
用Na2SO3溶液吸收硫酸工业尾气中的二氧化硫,将所得的混合液进行电解循环再生,这种新工艺叫再生循环脱硫法.其中阴、阳离子交换膜组合循环再生机理如图所示,则下列有关说法中正确的是( )| A、X为直流电源的正极,Y为直流电源的负极 |
| B、阳极区pH减小 |
| C、图中的b<a |
| D、阴极的电极反应为HSO3--2e-+H2O═SO42-+3H+和SO32--2e-+2H2O═SO42-+4H+ |
人的血液中存在H2CO3~HCO3-这样“一对”物质,前者的电离和后者的水解两个平衡使正常人血液的pH保持在7.35~7.45之间.血液中注射碱性物质时,上述电离和水解受到的影响分别是( )
| A、促进、促进 |
| B、促进、抑制 |
| C、抑制、促进 |
| D、抑制、抑制 |
下列对金、银、铜的描述错误的是( )
| A、金具有极高的抗腐蚀性、优良的导热、导电性 |
| B、银可用作有机合成催化剂、电池等材料 |
| C、Cu属于不活泼金属,在潮湿的空气中不易被腐蚀 |
| D、铜具有良好的导电性,大量用于制造电线、电缆 |
下列叙述正确的是( )
| A、离子晶体中,只存在离子键,不可能存在其它化学键 |
| B、在氧族元素(O、S、Se、Te)的氢化物中,水的沸点最低 |
| C、NaHSO4、Na2O2晶体中的阴阳离子个数比均为1:2 |
| D、晶体的熔点:金刚石>碳化硅>单晶硅 |