题目内容
I.已知在常温常压下:
①2CH3OH(l)十3O2(g)═2CO2(g)+4H2O(g)△H=-1275.6kJ?mol-1
②H2O(l)═H2O(g)△H=+44.0kJ?mol-1
写出表示甲醇燃烧热的热化学方程式 .
Ⅱ.磷酸(H3PO4)在水溶液中各种存在形式物质的量分数δ随pH的变化曲线如图1:
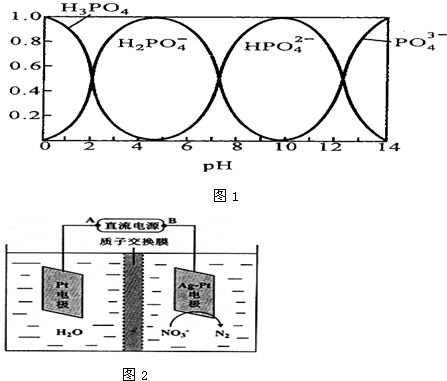
(1)在Na3PO4溶液中,
3(填“>”“=”“<”),向Na3PO4溶液中滴入稀盐酸后,pH从10降低到5的过程中发生的主要反应的离子方程式为 .
(2)从图1中推断NaH2PO4溶液中各种微粒浓度大小关系正确的是 .(填选项字母)
A、C(Na+)>C(H2PO4-)>C(H+)>C(HPO42-)>C(H3PO4)
B、C(Na+)>C(H2PO4-)>C(OH-)>C( H3PO4)>C(HPO42-)
C、C(H+)+C(Na+)=C(OH-)+C(H2PO4-)+2C(HPO42-)+3C(PO43-)+C(H3PO4)
D、C(Na+)=C(H2PO4-)+C(HPO42-)+C(PO43-)+C(H3PO4)
(3)假设25℃条件下测得0.1mol?L-1的Na3PO4溶液的pH=12,近似计算出Na3PO4的第一步水解的水解常数Kh(写出计算过程,忽略Na3PO4的第二、第三步水解,结果保留两位有效数字).
Ⅲ.化学在环境保护中起着十分重要的作用,电化学降解法可用于治理酸性水中的硝酸盐污染.电化学降解NO3-的原理如图2所示.电源正极为 (填A或B),阴极反应式为 .
①2CH3OH(l)十3O2(g)═2CO2(g)+4H2O(g)△H=-1275.6kJ?mol-1
②H2O(l)═H2O(g)△H=+44.0kJ?mol-1
写出表示甲醇燃烧热的热化学方程式
Ⅱ.磷酸(H3PO4)在水溶液中各种存在形式物质的量分数δ随pH的变化曲线如图1:

(1)在Na3PO4溶液中,
| c(Na+) |
| c(PO43-) |
(2)从图1中推断NaH2PO4溶液中各种微粒浓度大小关系正确的是
A、C(Na+)>C(H2PO4-)>C(H+)>C(HPO42-)>C(H3PO4)
B、C(Na+)>C(H2PO4-)>C(OH-)>C( H3PO4)>C(HPO42-)
C、C(H+)+C(Na+)=C(OH-)+C(H2PO4-)+2C(HPO42-)+3C(PO43-)+C(H3PO4)
D、C(Na+)=C(H2PO4-)+C(HPO42-)+C(PO43-)+C(H3PO4)
(3)假设25℃条件下测得0.1mol?L-1的Na3PO4溶液的pH=12,近似计算出Na3PO4的第一步水解的水解常数Kh(写出计算过程,忽略Na3PO4的第二、第三步水解,结果保留两位有效数字).
Ⅲ.化学在环境保护中起着十分重要的作用,电化学降解法可用于治理酸性水中的硝酸盐污染.电化学降解NO3-的原理如图2所示.电源正极为
考点:热化学方程式,原电池和电解池的工作原理,离子浓度大小的比较
专题:基本概念与基本理论
分析:Ⅰ、依据热化学方程式和盖斯定律计算所需热化学方程式;
Ⅱ、(1)磷酸钠中钠离子不水解、磷酸根离子水解;向Na3PO4溶液中滴入稀盐酸后,pH从10降低到5的过程中HPO42-浓度减小、H2PO4- 浓度增大;
(2)NaH2PO4溶液钠离子不水解、H2PO4- 水解和电离,溶液呈酸性,溶液中存在电荷守恒和物料守恒;
(3)依据水解离子方程式和平衡常数概念计算;
Ⅲ、根据图象知,硝酸根离子得电子发生氧化反应,则Ag-Pt作阴极,Pt电极为阳极,A为正极,B为负极,以此解答该题.
Ⅱ、(1)磷酸钠中钠离子不水解、磷酸根离子水解;向Na3PO4溶液中滴入稀盐酸后,pH从10降低到5的过程中HPO42-浓度减小、H2PO4- 浓度增大;
(2)NaH2PO4溶液钠离子不水解、H2PO4- 水解和电离,溶液呈酸性,溶液中存在电荷守恒和物料守恒;
(3)依据水解离子方程式和平衡常数概念计算;
Ⅲ、根据图象知,硝酸根离子得电子发生氧化反应,则Ag-Pt作阴极,Pt电极为阳极,A为正极,B为负极,以此解答该题.
解答:
解:I.①2CH3OH(l)十3O2(g)═2CO2(g)+4H2O(g)△H=-1275.6kJ?mol-1
②H2O(l)═H2O(g)△H=+44.0kJ?mol-1
依据盖斯定律①÷2-②×2得到:CH3OH(g)+
O2(g)=CO2(g)+2H2O(l)△H=-725.8kJ/mol;
故答案为:CH3OH(g)+
O2(g)=CO2(g)+2H2O(l)△H=-725.8kJ/mol;
II.(1)磷酸钠中钠离子不水解、磷酸根离子水解,所以
>3;向Na3PO4溶液中滴入稀盐酸后,pH从10降低到5的过程中HPO42-浓度减小、H2PO4- 浓度增大,所以发生的反应为 HPO42-+H+═H2PO4-,
故答案为:>;HPO42-+H+═H2PO4-;
(2)A、钠离子不水解,浓度最大,H2PO4-电离程度大于水解程度,溶液呈酸性,电离程度和水解程度都较小,所以溶液中存在C(Na+)>C(H2PO4-)>C(H+)>C(HPO42-)>C(H3PO4),故A正确;
B、H2PO4-电离程度大于水解程度,所以C(HPO42-)>C(H3PO4),故B错误;
C、溶液中存在电荷守恒C(H+)+C(Na+)=C(OH-)+C(H2PO4-)+2C(HPO42-)+3C(PO43-),故C错误;
D、溶液中存在物料守恒C(Na+)=C(H2PO4-)+C(HPO42-)+C(PO43-)+C(H3PO4),故D正确;
故选AD;
(3)依据化学平衡三段式计算 PO43-+H2O?HPO42-+OH-
起始浓度(mol?L-1):0.1 0 0
变化浓度(mol?L-1):0.01 0.01 0.01
平衡浓度(mol?L-1):0.09 0.01 0.01
Kh═
═
═1.1×10 -3mol?L-1;
答:Na3PO4的第一步水解的水解常数Kh为1.1×10 -3mol?L-1;
III. 由图示知在Ag-Pt电极上NO3-发生还原反应,因此Ag-Pt电极为阴极,则B为负极,A为电源正极,在阴极反应是NO3-得电子发生还原反应生成N2,利用电荷守恒与原子守恒知有H2O参与反应且有水生成,所以阴极上发生的电极反应式为:2NO3-+12H++10e-=N2+6H2O,
故答案为:A;2NO3-+10e-+12H+=6H2O+N2↑.
②H2O(l)═H2O(g)△H=+44.0kJ?mol-1
依据盖斯定律①÷2-②×2得到:CH3OH(g)+
| 3 |
| 2 |
故答案为:CH3OH(g)+
| 3 |
| 2 |
II.(1)磷酸钠中钠离子不水解、磷酸根离子水解,所以
| c(Na+) |
| c(PO43-) |
故答案为:>;HPO42-+H+═H2PO4-;
(2)A、钠离子不水解,浓度最大,H2PO4-电离程度大于水解程度,溶液呈酸性,电离程度和水解程度都较小,所以溶液中存在C(Na+)>C(H2PO4-)>C(H+)>C(HPO42-)>C(H3PO4),故A正确;
B、H2PO4-电离程度大于水解程度,所以C(HPO42-)>C(H3PO4),故B错误;
C、溶液中存在电荷守恒C(H+)+C(Na+)=C(OH-)+C(H2PO4-)+2C(HPO42-)+3C(PO43-),故C错误;
D、溶液中存在物料守恒C(Na+)=C(H2PO4-)+C(HPO42-)+C(PO43-)+C(H3PO4),故D正确;
故选AD;
(3)依据化学平衡三段式计算 PO43-+H2O?HPO42-+OH-
起始浓度(mol?L-1):0.1 0 0
变化浓度(mol?L-1):0.01 0.01 0.01
平衡浓度(mol?L-1):0.09 0.01 0.01
Kh═
| c(HP042-)×c(OH-) |
| c(PO43-) |
| 0.01×0.01 |
| 0.09 |
答:Na3PO4的第一步水解的水解常数Kh为1.1×10 -3mol?L-1;
III. 由图示知在Ag-Pt电极上NO3-发生还原反应,因此Ag-Pt电极为阴极,则B为负极,A为电源正极,在阴极反应是NO3-得电子发生还原反应生成N2,利用电荷守恒与原子守恒知有H2O参与反应且有水生成,所以阴极上发生的电极反应式为:2NO3-+12H++10e-=N2+6H2O,
故答案为:A;2NO3-+10e-+12H+=6H2O+N2↑.
点评:本题考查了电解原理,明确阴阳极上发生的电极反应及离子移动方向、阴阳极的判断方法等知识点即可解答,难点是电极反应式的书写盐类水解,根据溶液中的溶质及其溶液酸碱性来分析解答,根据电荷守恒、物料守恒确定离子浓度大小,难点是水解平衡常数的计算,利用三段式法解答,题目难度中等.

练习册系列答案
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案
相关题目
Q、W、X、Y、Z是原子序数依次增大的短周期元素,X的焰色反应呈黄色.Q元素的原子最外层电子数是其内层电子数的2倍.W、Z最外层电子数相同,Z的核电荷数是W的2倍.元素Y的合金是日常生活中使用最广泛的金属材料之一,下列说法正确的是( )
| A、原子半径的大小顺序:rX>rY>rW>rQ |
| B、X、Y的最高价氧化物的水化物之间不能发生反应 |
| C、元素Q和Z能形成QZ2型的共价化合物 |
| D、Z元素的氢化物稳定性大于W元素的氢化物稳定性 |
能正确表示下列反应的离子方程式的是( )
A、用铜作电极电解CuSO4溶液:2Cu2++2H2O
| ||||
| B、0.01mol/L NH4Al(SO4)2溶液与0.02 mol/L Ba(OH)2溶液等体积混合:A13++2SO42-+2Ba2++4OH-═2BaSO4↓+AlO2-+2H2O | ||||
| C、少量二氧化硫通入次氯酸钠碱性溶液中:SO2+ClO-+2OH-═SO42-+Cl-+H2O | ||||
| D、Ca(HCO3)2溶液与过量NaOH溶液反应:Ca2++HCO3-+OH-═CaCO3↓+H2O |
关于化学计量的应用,下列说法正确的是( )
| A、室温下,106g碳酸钠固体所含有的离子总的物质的量小于3mol |
| B、在同压不同温的情况下,质量相同的氧气和臭氧所含氧原子数不相同 |
| C、将物质的量浓度分别为1mol/L和2mol/L的硫酸等质量混合(假设体积可以加和),则混合后硫酸溶液的浓度为1.5mol/L |
| D、标况下,22.4L CH3Cl分子数约为6.02×1023 |
在10L恒容密闭容器中充入X(g)和Y(g),发生反应X(g)+Y(g)?M(g)+N(g),所得实验数据如表:
下列说法正确的是( )
| 实验编号 | 温度/℃ | 起始时物质的量/mol | 平衡时物质的量/mol | |
| n(X) | n(Y) | n(M) | ||
| ① | 700 | 0.40 | 0.10 | 0.090 |
| ② | 800 | 0.10 | 0.40 | 0.080 |
| ③ | 800 | 0.20 | 0.30 | a |
| ④ | 900 | 0.10 | 0.15 | b |
| A、实验①中,若5min时测得n(M)=0.050mol,则0至5min时间内,用N表示的平均反应速率v(N)=1.0×10-2mol/(L?min) |
| B、实验②中,该反应的平衡常数K=2.0 |
| C、实验③中,达到平衡时,X的转化率为60% |
| D、实验④中,达到平衡时,b>0.060 |
下列图示实验现象及其解释不正确的是( )
A、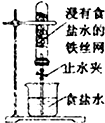 一段时间后打开止水夹,观察到导管中液面上升,因为铁发生了吸氧腐蚀 |
B、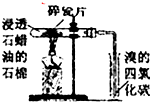 加热一段时间,观察到溴的四氯化碳溶液颜色褪去,因为有气态烯烃产生 |
C、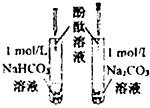 溶液均变红,碳酸钠溶液颜色较深,因为相同条件下水解能力HCO3-强于CO32- |
D、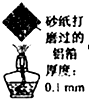 加热一段时间,观察到熔化的铝未滴落,因为铝表面生成氧化铝的熔点很高 |
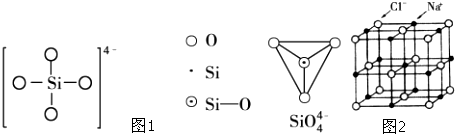
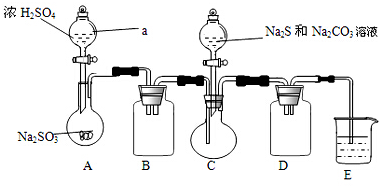
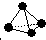 ,已知断裂1mol N-N键吸收167kJ的热量,生成1mol N≡N键放出942kJ热量.试判断相同条件下N4与N2的稳定性顺序是:
,已知断裂1mol N-N键吸收167kJ的热量,生成1mol N≡N键放出942kJ热量.试判断相同条件下N4与N2的稳定性顺序是: