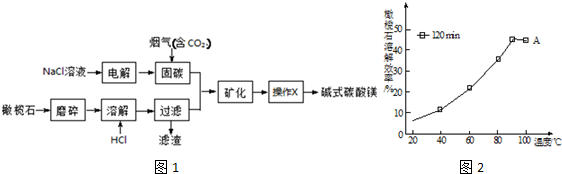
题目内容
17.下列说法不正确的是( )| A. | 压减燃煤、严格控车、调整产业是治理雾霾的有效措施 | |
| B. | 铝及其合金使用广泛,是因为铝比铁更耐酸、碱的腐蚀 | |
| C. | 海水淡化的方法主要有蒸馏法、电渗析法、离子交换法等 | |
| D. | 通常所说的三大合成材料是指塑料、合成橡胶和合成纤维 |
分析 A.汽车尾气中含有烟尘等颗粒物,化石燃料的燃烧等都会产生大气的污染,调整产业结构,尽量减少对化石燃料的使用,能够减少雾霾;
B.铝易于碱性溶液发生反应;
C.海水淡化主要目的除去海水中盐,常用的方法有:蒸馏法、电渗析法、离子交换法;
D.合成材料为高分子化合物,主要有三大类:塑料、合成纤维、合成橡胶.
解答 解:A.汽车尾气中含有燃料不充分燃烧产生的烟尘等,污染了空气,能引起大气中PM2.5增大,化石燃料燃烧会产生CO、SO2和粉尘等有害气体,污染了空气,能引起大气中PM2.5增大,产生雾霾天气,调整产业结构,尽量减少对化石燃料的使用,能够减少雾霾,故A正确;
B.铝能够与碱反应,容易被碱腐蚀,故B错误;
C.海水淡化的主要方法有:蒸馏法、电渗析法、离子交换法等,故C正确;
D.三大合成材料是指塑料、合成橡胶和合成纤维,故D正确;
故选:B.
点评 本题为综合题,考查了环境污染与治理、合金的性质、海水淡化的方法、材料的分类,题目难度不大,试题涉及的知识点较多,充分考查了学生的分析、理解能力及灵活应用所学知识的能力.

练习册系列答案
相关题目
7.用0.1mol•L-1NaOH溶液滴定25mL0.1mol•L-1CH3COOH溶液滴定曲线如下图①;用0.1mol•L-1盐酸滴定25mL0.1mol•L-1氨水的滴定曲线分别如下图②所示.下列有关说法不正确的是( )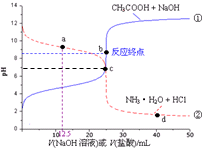

| A. | a点:c(Cl-)>c(NH3•H2O)>c(NH4+) | B. | b点:c(OH-)=c(H+)+c(CH3COOH) | ||
| C. | c点:c(NH4+)=c(CH3COO-) | D. | d点:c(NH4+)>c(Cl-)>c(H+) |
5.利用下列实验装置能完成相应实验的是( )
| A. |  制取并收集干燥纯净的NH3 | |
| B. |  用该装置分离乙酸乙酯和饱和碳酸钠溶液 | |
| C. |  用于制备并收集少量NO2 | |
| D. |  比较MnO2、Cl2、S的氧化性 |
2.现有常温下pH=2的盐酸甲和pH=2的醋酸溶液乙,请根据下列操作回答问题:
(1)常温下0.1mol/L的CH3COOH溶液加水稀释过程,下列表达式的数据一定增大的是BD.
A.c(H+) B.$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$ C.c(H+)•c(OH-) D.$\frac{c(O{H}^{-})}{c({H}^{+})}$
(2)取10mL的乙溶液,加入等体积的水,醋酸的电离平衡向右(填“向左”、“向右”或“不”)移动;另取10mL的乙溶液,加入少量无水醋酸钠固体(假设加入固体前后,溶液体积保持不变),待固体溶解后,溶液中$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$ 的比值将减小(填“增大”、“减小”或“无法确定”).
(3)取等体积的甲、乙两溶液,分别用等浓度的NaOH稀溶液中和,则消耗的NaOH溶液的体积大小关系为:V(甲)< V(乙) ( 填“>”、“<”或“=”).
(4)已知25℃时,两种酸的电离平衡常数如下:
下列四种离子结合H+能力最强的是B.
A.HCO3- B.CO32- C.ClO- D.CH3COO-
(5)常温下,取甲溶液稀释100倍,其pH=4;取99mL甲溶液与1mL1mol/L的NaOH溶液混合(忽略溶液体积变化),恢复至常温时其pH=10.
(1)常温下0.1mol/L的CH3COOH溶液加水稀释过程,下列表达式的数据一定增大的是BD.
A.c(H+) B.$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$ C.c(H+)•c(OH-) D.$\frac{c(O{H}^{-})}{c({H}^{+})}$
(2)取10mL的乙溶液,加入等体积的水,醋酸的电离平衡向右(填“向左”、“向右”或“不”)移动;另取10mL的乙溶液,加入少量无水醋酸钠固体(假设加入固体前后,溶液体积保持不变),待固体溶解后,溶液中$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$ 的比值将减小(填“增大”、“减小”或“无法确定”).
(3)取等体积的甲、乙两溶液,分别用等浓度的NaOH稀溶液中和,则消耗的NaOH溶液的体积大小关系为:V(甲)< V(乙) ( 填“>”、“<”或“=”).
(4)已知25℃时,两种酸的电离平衡常数如下:
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数K1 | 1.8×10-5 | 4.3×10-7 | 3.0×10-8 |
| K2 | -- | 5.6×10-11 | -- |
A.HCO3- B.CO32- C.ClO- D.CH3COO-
(5)常温下,取甲溶液稀释100倍,其pH=4;取99mL甲溶液与1mL1mol/L的NaOH溶液混合(忽略溶液体积变化),恢复至常温时其pH=10.
9.如图是部分短周期元素原子(用字母表示)最外层电子数与原子序数的关系,下列说法正确的是( )
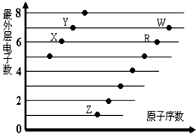

| A. | X与Z两种元素形成的化合物一定是离子化合物,有且只有离子键 | |
| B. | RX2、WX2、Z2X2都能使品红溶液褪色,且褪色原理相同 | |
| C. | R、W所形成的氧化物的水化物的酸性强弱为W>R | |
| D. | X、Y、R、W四种元素形成的气体氢化物中最稳定的是 Y 的气态氢化物 |
6.糖类、油脂、蛋白质是重要的营养物质,下列说法正确的是( )
| A. | 糖类都能够发生水解 | |
| B. | 蛋白质的水解产物都含有羧基和羟基 | |
| C. | 油脂碱性水解可以制取肥皂和甘油 | |
| D. | 它们都属于高分子化合物 |
3.某小组通过实验研究Na2O2与水的反应.
(1)Na2O2与水反应的化学方程式2Na2O2+2H2O=4NaOH+O2↑
(2)ⅱ中溶液褪色可能是溶液a中存在较多的H2O2与酚酞发生了反应.
Ⅰ.甲同学通过实验证实了H2O2的存在:取少量溶液a,加入试剂MnO2(填化学式),有气体产生.
Ⅱ.乙同学查阅资料获悉:用KMnO4可以测定H2O2的含量:取15.00mL溶液a,用稀H2SO4酸化,逐滴加入0.003mol•L-1KMnO4溶液,产生气体,溶液褪色速率开始较慢后变快,至终点时共消耗20.00mLKMnO4溶液.
①请配平:2MnO4-+5H2O2+6H+═2Mn2++5O2↑+8H2O
②溶液a中c(H2O2)=0.01mol•L-1.
③溶液褪色速率开始较慢后变快的原因可能是反应生成的Mn2+作催化剂.
(3)为探究现象ⅱ产生的原因,同学们继续进行了如下实验:
Ⅲ.向H2O2溶液中滴入两滴酚酞,振荡,加入5滴0.1mol•L-1NaOH溶液,溶液变红又迅速变无色且产生气体,10分钟后溶液变无色.
Ⅳ.向0.1mol•L-1NaOH溶液中滴入两滴酚酞的,振荡,溶液变红,10分钟后溶液颜色无明显变化;向该溶液中通入O2,溶液颜色无明显变化.
①从实验Ⅲ和Ⅳ中,可得出的结论是碱性条件下,H2O2能与酚酞反应而O2不能.
②同学们进一步通过实验证实了溶液a中滴入酚酞后,H2O2与酚酞发生了化学反应.实验方案是:取少量溶液a于试管中,加入MnO2,充分反应后,向上层清液中滴入2滴酚酞后变红,10分钟后,溶液颜色无明显变化.
| 操作 | 现象 |
| 向盛有4gNa2O2的烧杯中加入50mL蒸馏水得到溶液a | 剧列反应,产生能使带火星木条复燃的气体 |
| 取5mL溶液a于试管中,滴入两滴酚酞 | ⅰ.溶液变红 ⅱ.10分种后溶液颜色明显变浅,稍后,溶液变为无色 |
(2)ⅱ中溶液褪色可能是溶液a中存在较多的H2O2与酚酞发生了反应.
Ⅰ.甲同学通过实验证实了H2O2的存在:取少量溶液a,加入试剂MnO2(填化学式),有气体产生.
Ⅱ.乙同学查阅资料获悉:用KMnO4可以测定H2O2的含量:取15.00mL溶液a,用稀H2SO4酸化,逐滴加入0.003mol•L-1KMnO4溶液,产生气体,溶液褪色速率开始较慢后变快,至终点时共消耗20.00mLKMnO4溶液.
①请配平:2MnO4-+5H2O2+6H+═2Mn2++5O2↑+8H2O
②溶液a中c(H2O2)=0.01mol•L-1.
③溶液褪色速率开始较慢后变快的原因可能是反应生成的Mn2+作催化剂.
(3)为探究现象ⅱ产生的原因,同学们继续进行了如下实验:
Ⅲ.向H2O2溶液中滴入两滴酚酞,振荡,加入5滴0.1mol•L-1NaOH溶液,溶液变红又迅速变无色且产生气体,10分钟后溶液变无色.
Ⅳ.向0.1mol•L-1NaOH溶液中滴入两滴酚酞的,振荡,溶液变红,10分钟后溶液颜色无明显变化;向该溶液中通入O2,溶液颜色无明显变化.
①从实验Ⅲ和Ⅳ中,可得出的结论是碱性条件下,H2O2能与酚酞反应而O2不能.
②同学们进一步通过实验证实了溶液a中滴入酚酞后,H2O2与酚酞发生了化学反应.实验方案是:取少量溶液a于试管中,加入MnO2,充分反应后,向上层清液中滴入2滴酚酞后变红,10分钟后,溶液颜色无明显变化.