题目内容
12.工业上利用橄榄石(主要成分是Mg2SiO4)固定CO2,生产碱式碳酸镁[Mg2(OH)2CO3]的工艺流程如图1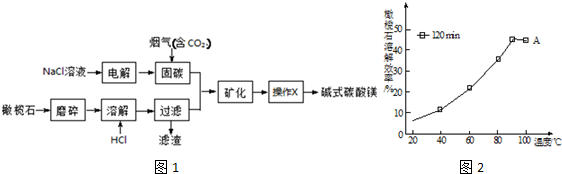
已知:Mg2SiO4(s)+4HCl(aq)═2MgCl2(aq)+SiO2(s)+2H2O(l)△H=-49.04 kJ•mol-1
(1)某橄榄石的组成是(MgFe)2(SiO4)2,用氧化物的形式可表示为MgO•FeO•SiO2.
(2)固碳(足量的CO2)时主要反应的离子方程式为OH-+CO2=HCO3-.
下列物质中也可用作“固碳”的是ad (填字母).
a.(NH4)2CO3溶液 b.BaCl2溶液 c.NH4HCO3 d.氨水
(3)矿化的离子方程式为2Mg 2++4HCO3-=Mg2(OH)2CO3↓+H2O+3CO2↑或2Mg 2++2CO32-+H2O=Mg2(OH)2CO3↓+CO2↑;分离出碱式碳酸镁的操作X为过滤.
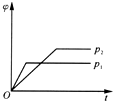
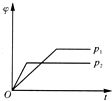
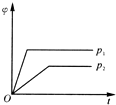
(4)流程中将橄榄石磨碎后再进行溶解的目的是增大接触面积,加快溶解速率,研究表明,用一定量一定浓度的盐酸,在不同温度时,测得溶解橄榄石的效率随温度变化情况如图2所示(时间都为120min),试分析90℃橄榄石溶解效率开始降低的原因90℃、120min时,溶解达到平衡,而反应放热,升温平衡逆向移动,故溶解效率降低.
(5)若该工厂排放烟气的速率为22.4m3/min(已换成标准状况下),其中CO2的体积分数为10%,则理论上此工厂1小时可制得碱式碳酸镁852 kg.
分析 橄榄石磨碎后溶解,然后加入HCl,发生的反应为Mg2SiO4+4HCl═2MgCl2+SiO2+2H2O,过滤,得到滤液;氯化钠溶液电解生成氯气、氢气和NaOH,通入烟气后能固碳,应该是NaOH和二氧化碳反应生成碳酸钠或碳酸氢钠,碳酸钠和氯化镁或碳酸氢钠和氯化镁反应生成碱式碳酸镁,然后过滤得到碱式碳酸镁,
(1)某橄榄石的组成是(MgFe)2(SiO4)2,用氧化物的形式表示时,先写活泼金属氧化物、后写较不活泼金属氧化物,最后写二氧化硅;
(2)固碳(足量的CO2)时氢氧根离子和二氧化碳反应生成碳酸氢根离子;
能和烟气反应生成可溶性碳酸盐的物质能固碳;
(3)矿化的反应为镁离子和碳酸氢根离子或碳酸根离子的反应;分离难溶性固体和溶液采用过滤方法;
(4)反应物接触面积越大,反应速率越快;该反应是放热反应,温度越高其转化率越小;
(5)每小时烟气中n(CO2)=$\frac{22.4{m}^{3}/min×60min×10%×1000L/{m}^{3}}{22.4L/mol}$=6000mol,再根据二氧化碳和碱式碳酸镁之间的关系式计算.
解答 解:橄榄石磨碎后溶解,然后加入HCl,发生的反应为Mg2SiO4+4HCl═2MgCl2+SiO2+2H2O,过滤,得到滤液;氯化钠溶液电解生成氯气、氢气和NaOH,通入烟气后能固碳,应该是NaOH和二氧化碳反应生成碳酸钠或碳酸氢钠,碳酸钠和氯化镁或碳酸氢钠和氯化镁反应生成碱式碳酸镁,然后过滤得到碱式碳酸镁,
(1)某橄榄石的组成是(MgFe)2(SiO4)2,用氧化物的形式表示时,先写活泼金属氧化物、后写较不活泼金属氧化物,最后写二氧化硅,所以其氧化物的形式为MgO•FeO•SiO2,故答案为:MgO•FeO•SiO2;
(2)固碳(足量的CO2)时氢氧根离子和二氧化碳反应生成碳酸氢根离子,离子方程式为OH-+CO2=HCO3-;
能和烟气反应生成可溶性碳酸盐的物质能固碳,符合条件的只有ad,
故答案为:OH-+CO2=HCO3-;ad;
(3)矿化的反应为镁离子和碳酸氢根离子或碳酸根离子的反应,离子方程式为2Mg 2++4HCO3-=Mg2(OH)2CO3↓+H2O+3CO2↑或2Mg 2++2CO32-+H2O=Mg2(OH)2CO3↓+CO2↑;分离难溶性固体和溶液采用过滤方法,所以该操作方法是过滤,
故答案为:2Mg 2++4HCO3-=Mg2(OH)2CO3↓+H2O+3CO2↑或2Mg 2++2CO32-+H2O=Mg2(OH)2CO3↓+CO2↑;过滤;
(4)反应物接触面积越大,反应速率越快,粉碎的目的是增大反应物接触面积,加快反应速率;该反应是放热反应,温度越高其转化率越小,所以90℃、120min时,溶解达到平衡,而反应放热,升温平衡逆向移动,故溶解效率降低,
故答案为:增大接触面积,加快溶解速率;90℃、120min时,溶解达到平衡,而反应放热,升温平衡逆向移动,故溶解效率降低;
(5)每小时烟气中n(CO2)=$\frac{22.4{m}^{3}/min×60min×10%×1000L/{m}^{3}}{22.4L/mol}$=6000mol,
根据C原子守恒得n(CO2)=n[Mg2(OH)2CO3]=6000mol,则得到的碱式碳酸镁的质量=6000mol×142g/mol=852000g=852kg,故答案为:852.
点评 本题考查物质制备,为高频考点,侧重考查学生分析、判断、计算及知识综合运用能力,涉及化学方程式的计算、反应速率影响因素、物质分离和提纯、离子方程式的书写等知识点,明确基本原理、元素化合物性质、物质分离和提纯方法是解本题关键,题目难度不大.

①合成氨 ②塑料 ③合成盐酸 ④合成橡胶 ⑤合成尿素 ⑥合成纤维 ⑦合成洗涤剂.
| A. | ②④⑦ | B. | ②④⑥ | C. | ①③⑤ | D. | ④⑤⑥ |
| A. | 压减燃煤、严格控车、调整产业是治理雾霾的有效措施 | |
| B. | 铝及其合金使用广泛,是因为铝比铁更耐酸、碱的腐蚀 | |
| C. | 海水淡化的方法主要有蒸馏法、电渗析法、离子交换法等 | |
| D. | 通常所说的三大合成材料是指塑料、合成橡胶和合成纤维 |
| A. | NH3$→_{催化剂△}^{O_{2}}$NO$→_{H_{2}O}^{O_{2}}$HNO3 | |
| B. | 浓HCl$→_{△}^{MnO_{2}}$Cl2$\stackrel{石灰乳}{→}$漂白粉 | |
| C. | Al2O3$\stackrel{HCl(aq)}{→}$AlCl3(aq)$\stackrel{△}{→}$无水AlCl3$\stackrel{电解}{→}$Al | |
| D. | 淀粉$→_{△}^{H_{2}SO_{4}(aq)}$葡萄糖$\stackrel{酒化酶}{→}$C2H5OH$→_{Ag,△}^{O_{2}}$CH3CHO |
| A. | Na2SO4 | B. | FeCl3 | C. | NaHCO3 | D. | CH3COOH |
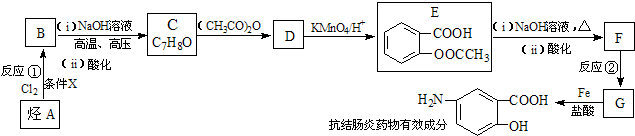
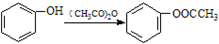
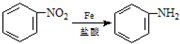
 ;
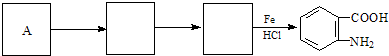
;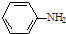 )易被氧化,苯环上连有烷基时再引入一个取代基,常取代在烷基的邻对位,而当苯环上连有羧基时则取代在间位.据此按先后顺序写出以A为原料合成邻氨基苯甲酸(
)易被氧化,苯环上连有烷基时再引入一个取代基,常取代在烷基的邻对位,而当苯环上连有羧基时则取代在间位.据此按先后顺序写出以A为原料合成邻氨基苯甲酸( 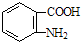 )合成路线中两种中间产物的结构简式(部分反应条件已略去)
)合成路线中两种中间产物的结构简式(部分反应条件已略去)