题目内容
5.利用下列实验装置能完成相应实验的是( )| A. |  制取并收集干燥纯净的NH3 | |
| B. |  用该装置分离乙酸乙酯和饱和碳酸钠溶液 | |
| C. |  用于制备并收集少量NO2 | |
| D. |  比较MnO2、Cl2、S的氧化性 |
分析 A.氨气应用向下排空气法收集;
B.乙酸乙酯和饱和碳酸钠不溶;
C.二氧化氮能与水反应生成NO;
D.用浓盐酸和二氧化锰制备氯气,应在加热条件下进行.
解答 解:A.氨气密度比空气小,应用向下排空气法收集,故A错误;
B.乙酸乙酯和饱和碳酸钠不溶,能分层,可用分液分离,故B正确;
C.二氧化氮能与水反应生成NO,不能用排水法收集,故C错误;
D.用浓盐酸和二氧化锰制备氯气,应在加热条件下进行,故D错误.
故选B.
点评 本题考查化学实验方案评价,为高频考点,侧重考查仪器的选取,明确实验原理及操作步骤是解本题关键,结合仪器的作用分析解答,注意从实验操作的规范性及仪器作用解答,易错选项是C.

练习册系列答案
相关题目
15.有A,B两种有机物,可能是烃或烃的含氧衍生物,已知它们含氢的质量分数相等.关于A和B的下列叙述不正确的是( )
| A. | A和B可能是同分异构体 | |
| B. | A和B的最简式可能相同 | |
| C. | A和B不可能一个是烃,一个是烃的含氧衍生物 | |
| D. | 将A和B混合,当混合物质量一定时,无论A、B以何种比例混合,完全燃烧时产生的H2O的量均相等 |
16.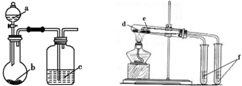 用图所示装置进行实验,能得出相应实验结论的是( )
用图所示装置进行实验,能得出相应实验结论的是( )
 用图所示装置进行实验,能得出相应实验结论的是( )
用图所示装置进行实验,能得出相应实验结论的是( )| 选项 | 实验试剂 | 实验结论 | ||
| A | a.稀硫酸 | b.碳酸氢钠 | c.硅酸钠溶液 | 酸性:硫酸>碳酸>硅酸 |
| B | a.稀盐酸 | b.二氧化锰 | c.溴化钠溶液 | 氧化性:MnO2>Cl2>Br2 |
| C | d.小苏打 | e.苏打 | f.石灰水 | 热稳定性:苏打>小苏打 |
| D | d.氯化钠 | e.氯化铵 | f.硝酸银溶液 | 沸点:氯化钠>氯化铵 |
| A. | A | B. | B | C. | C | D. | D |
13.关于能量转化的叙述不正确的是( )
| A. | 反应物总能量高于生成物的总能量的反应为放热反应 | |
| B. | 化学键的断裂和形成是化学反应中能量变化的主要原因 | |
| C. | 只有氧化还原反应中的化学能才有可能转化为电能---形成原电池 | |
| D. | 需要加热才能发生的反应都是吸热反应 |
20.现代以石油化工为基础的三大合成材料是( )
①合成氨 ②塑料 ③合成盐酸 ④合成橡胶 ⑤合成尿素 ⑥合成纤维 ⑦合成洗涤剂.
①合成氨 ②塑料 ③合成盐酸 ④合成橡胶 ⑤合成尿素 ⑥合成纤维 ⑦合成洗涤剂.
| A. | ②④⑦ | B. | ②④⑥ | C. | ①③⑤ | D. | ④⑤⑥ |
17.下列说法不正确的是( )
| A. | 压减燃煤、严格控车、调整产业是治理雾霾的有效措施 | |
| B. | 铝及其合金使用广泛,是因为铝比铁更耐酸、碱的腐蚀 | |
| C. | 海水淡化的方法主要有蒸馏法、电渗析法、离子交换法等 | |
| D. | 通常所说的三大合成材料是指塑料、合成橡胶和合成纤维 |
14.Wolff-Kishner-黄鸣龙反应是醛类或酮类在碱性条件下与肼作用,使得>C═O转化为-CH2-.如:
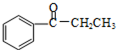 +H2N-NH2$→_{△}^{NaOH/(HOCH_{2}CH_{2})_{2}O}$
+H2N-NH2$→_{△}^{NaOH/(HOCH_{2}CH_{2})_{2}O}$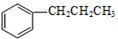 +X(g)+Y(l)
+X(g)+Y(l)
其中,X和Y不污染环境,下列说法中不正确的是( )
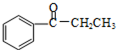 +H2N-NH2$→_{△}^{NaOH/(HOCH_{2}CH_{2})_{2}O}$
+H2N-NH2$→_{△}^{NaOH/(HOCH_{2}CH_{2})_{2}O}$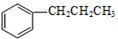 +X(g)+Y(l)
+X(g)+Y(l)其中,X和Y不污染环境,下列说法中不正确的是( )
| A. | 肼作还原剂 | B. | X是N2 | ||
| C. | Y是H2O | D. | 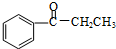 在酸性条件下水解为苯甲酸和乙醇 在酸性条件下水解为苯甲酸和乙醇 |
11.(1)下图所示元素周期表中全部是金属元素的区域为B
A.A B.B C.C D.D
(2)现有甲、乙两种短周期元素,室温下,甲元素单质在冷浓硫酸或空气中,表面都生成致密的氧化膜,乙元素原子核外M电子层与K电子层上的电子数相等.
甲、乙两元素相比较,金属性较强的是镁(填名称),可以验证该结论的实验是BC.
A.将在空气中放置很久的这两种元素的块状单质分别放入热水中
B.将这两元素的单质粉末分别和同浓度的盐酸反应
C.将这两元素的单质粉末分别和热水作用,并滴入酚酞
D.比较这两种元素的气态氢化物的稳定性
(3)上表中所列某些元素间能形成等电子的A、B、C、D、E五种微粒,A与C组成元素相同,B、E、D组成元素相同,它们间能发生如下反应:A+B=C+D,E+B=2D,则写出E的电子式: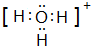
(4)“神舟六号”载人飞船舱内有一种化合物来吸收航天员呼出的CO2,你认为该物质是由上表中c、f(填字母)元素组成的,写出该反应的化学方程式2Na2O2+2CO2═2Na2CO3+CO2.
A.A B.B C.C D.D
| a | b | ||||||||||||||||
| d | e | f | |||||||||||||||
| c | g | h | |||||||||||||||
| A | B | C | D | ||||||||||||||
甲、乙两元素相比较,金属性较强的是镁(填名称),可以验证该结论的实验是BC.
A.将在空气中放置很久的这两种元素的块状单质分别放入热水中
B.将这两元素的单质粉末分别和同浓度的盐酸反应
C.将这两元素的单质粉末分别和热水作用,并滴入酚酞
D.比较这两种元素的气态氢化物的稳定性
(3)上表中所列某些元素间能形成等电子的A、B、C、D、E五种微粒,A与C组成元素相同,B、E、D组成元素相同,它们间能发生如下反应:A+B=C+D,E+B=2D,则写出E的电子式:
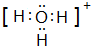
(4)“神舟六号”载人飞船舱内有一种化合物来吸收航天员呼出的CO2,你认为该物质是由上表中c、f(填字母)元素组成的,写出该反应的化学方程式2Na2O2+2CO2═2Na2CO3+CO2.
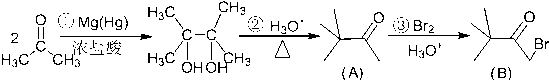
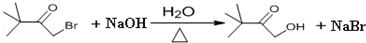 .
.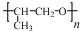 ,则该同分异构体的结构简式为:
,则该同分异构体的结构简式为: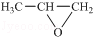 .
.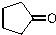 )来代替丙酮,连续发生上述路线中反应①、②之后,得到的有机产物的结构简式为:
)来代替丙酮,连续发生上述路线中反应①、②之后,得到的有机产物的结构简式为: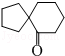 .
.