题目内容
6.A、B、C、D四种元素,它们原子的核电荷数均小于18,且依次递增,A原子核内仅有一个质子;B原子的电子总数与D原子的最外层电子数相等;A原子与B原子的最外层电子数之和与C原子的最外层电子数相等;D原子有两个电子层,最外层电子数是次外层电子数的3倍.(1)写出元素符号:AH,BC,CN.
(2)画出D的离子结构示意图
 .
.
分析 A、B、C、D四种元素,它们原子的核电荷数均小于18,且依次递增.A原子核内仅有1个质子,则A为H元素;D原子的最外层电子数是次外层电子数的3倍,最外层电子数不超过8,原子只能有2个电子层,最外层电子数为6,故D为O元素;B原子的电子总数与D原子的最外层电子数相等,则B为C元素;A原子与B原子的最外层电子数之和与C原子的最外层电子数相等,则C原子最外层电子数为1+4=5,其原子序数小于氧,故C为N元素,以此解答该题.
解答 解:(1)由以上分析可知A为H,B为C,C为N 元素,故答案为:H;C;N;
(2)D为O元素,对应离子核外有2个电子层,最外层电子数为8,则结构示意图为 ,故答案为:
,故答案为: .
.
点评 本题考查结构与位置关系,为高频考点,侧重考查学生的分析能力,关键是熟练掌握短周期元素,理解掌握核外电子排布规律,有利于基础知识的巩固.

练习册系列答案
 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案
相关题目
13.在2L的密闭容器中,一定条件下发生化学反应:2NO(g)+2CO(g)═2CO2(g)+N2(g).起始反应时NO和CO各为4mol,10s后达到化学平衡,测得N2为1mol.下列有关说法中正确的是( )
| A. | 在其他条件不变时,增加压强,N2的体积分数不变 | |
| B. | 前5 s内,用CO表示的反应速率等于0.1 mol•L-1•s-1 | |
| C. | 10 s时密闭容器中压强维持不变 | |
| D. | 保持容器体积不变,往容器中充入1 mol O2,正、逆反应速率都不改变 |
14.下列关于常见物质的工业制法的叙述,不正确的是( )
| A. | 工业制硅:用焦炭在高温下还原二氧化硅可制得高纯硅 | |
| B. | 工业冶炼铁:需要用到的原料有铁矿石、焦炭、空气和石灰石 | |
| C. | 工业冶炼镁:电解熔融的无水氯化镁,可以得到金属镁 | |
| D. | 工业制玻璃:将石灰石、纯碱、石英在玻璃熔炉中高温熔融制得 |
11.下列说法正确的是( )
| A. | 将塑料废弃物加工成防水材料或汽油,变废为宝 | |
| B. | 煤燃烧产生的烟气直接排放到空气中,易造成水体的富营养化 | |
| C. | 食品添加剂必须用天然物质制造 | |
| D. | 乙醇、过氧化氢、次氯酸钠等消毒液均可以将病毒氧化而达到消毒的目的 |
11.下列有关气体体积的叙述中,正确的是( )
| A. | 一定温度和压强下,各种气态物质体积的大小,由构成气体的分子大小决定 | |
| B. | 不同的气体,若体积相同,则它们所含的分子数必相同 | |
| C. | 气体的摩尔体积是指1mol任何气体所占的体积都是22.4L | |
| D. | 恒温恒压条件下,反应前后气体的体积之比等于气体的物质的量之比 |
18.把6moLM和5moLN的混合气体通入容积为4L的密闭容器中,在一定条件下发生如下反应:5M(g)+4N(g)?6P(g)+xQ(g),经5min后反应达到平衡,此时生成P 3moL,并测得Q的平均反应速率为0.1mol/(L•min)下列说法正确的是( )
| A. | 化学计量数x=2 | B. | M的转化率为41.67% | ||
| C. | N的平衡浓度为0.075mol/L | D. | 反应前后混合气体的压强比为$\frac{23}{22}$ |
15.下列物质在生活中有广泛应用,其中不属于离子化合物的是( )
| A. | NO | B. | Ca(ClO)2 | C. | NaCl | D. | NaHCO3 |
16.下列化学方程式书写正确的是( )
| A. | nCH2=CH2$\stackrel{催化剂}{→}$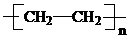 | |
| B. | CH2=CH2+Br2→CH3CHBr2 | |
| C. | 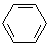 +HNO3$→_{60℃}^{浓硫酸}$ +HNO3$→_{60℃}^{浓硫酸}$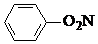 +H2O +H2O | |
| D. | CH3COOH+CH3CH2OH$?_{△}^{浓H_{2}SO_{4}}$CH3COOCH3CH2+H2O |
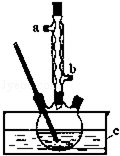 正丁醚(CH3CH2CH2CH2OCH2CH2CH2CH3)是一种化工原料,常温下为无色液体,不溶于水,沸点为142.4℃,密度比水小.某实验小组利用如下装置合成正丁醚(其它装置均略去),发生的主要反应为:
正丁醚(CH3CH2CH2CH2OCH2CH2CH2CH3)是一种化工原料,常温下为无色液体,不溶于水,沸点为142.4℃,密度比水小.某实验小组利用如下装置合成正丁醚(其它装置均略去),发生的主要反应为: