题目内容
实验室用NaOH固体配制250mL 1.25mol/L的NaOH溶液,填空并请回答下列问题:
(1)配制250mL 1.25mol/L的NaOH溶液
(2)容量瓶上需标有以下五项中的 ;①温度 ②浓度 ③容量 ④压强 ⑤刻度线
(3)配制时,其正确的操作顺序是(字母表示,每个字母只能用一次) ;
A、用30mL水洗涤烧杯2-3次,洗涤液均注入容量瓶,振荡
B、用天平准确称取所需的NaOH的质量,加入少量水(约30mL),用玻璃棒慢慢搅动,使其充分溶解
C、将已冷却的NaOH溶液沿玻璃棒注入250mL的容量瓶中
D、将容量瓶盖紧,颠倒摇匀
E、改用胶头滴管加水,使溶液凹面恰好与刻度相切
F、继续往容量瓶内小心加水,直到液面接近刻度1-2cm处
(4)操作A中,将洗涤液都移入容量瓶,其目的是 ,溶液注入容量瓶前需恢复到室温,这是因为 .
(1)配制250mL 1.25mol/L的NaOH溶液
| 应称取NaOH的质量/g | 应选用容量瓶的规格/mL | 除容量瓶外还需要的其它玻璃仪器 |
(3)配制时,其正确的操作顺序是(字母表示,每个字母只能用一次)
A、用30mL水洗涤烧杯2-3次,洗涤液均注入容量瓶,振荡
B、用天平准确称取所需的NaOH的质量,加入少量水(约30mL),用玻璃棒慢慢搅动,使其充分溶解
C、将已冷却的NaOH溶液沿玻璃棒注入250mL的容量瓶中
D、将容量瓶盖紧,颠倒摇匀
E、改用胶头滴管加水,使溶液凹面恰好与刻度相切
F、继续往容量瓶内小心加水,直到液面接近刻度1-2cm处
(4)操作A中,将洗涤液都移入容量瓶,其目的是
考点:配制一定物质的量浓度的溶液
专题:物质的量浓度和溶解度专题
分析:(1)根据n=cV和m=nM来计算;根据容量瓶只有一条刻度线,只能配制与其规格相对应的体积的溶液;根据配制步骤是计算、称量、溶解、移液、洗涤、定容、摇匀、装瓶来分析需要的仪器;
(2)据容量瓶的使用方法分析,容量瓶是用来配制一定物质的量浓度溶液的定量容器,只能在常温下使用,不能用来盛装过冷或过热的液体,不能用来稀释溶液或作为反应容器.
(3)根据配制步骤是计算、称量、溶解、冷却、移液、洗涤、定容、摇匀、装瓶来对操作顺序进行排序;
(4)烧杯和玻璃棒上都沾有硫酸,洗涤液中含有少量的溶质,为避免溶质的量的减少,应将洗涤液全部转移到容量瓶中,当溶液没冷却至室温时即定容,则冷却后溶液体积会偏小,影响浓度.
(2)据容量瓶的使用方法分析,容量瓶是用来配制一定物质的量浓度溶液的定量容器,只能在常温下使用,不能用来盛装过冷或过热的液体,不能用来稀释溶液或作为反应容器.
(3)根据配制步骤是计算、称量、溶解、冷却、移液、洗涤、定容、摇匀、装瓶来对操作顺序进行排序;
(4)烧杯和玻璃棒上都沾有硫酸,洗涤液中含有少量的溶质,为避免溶质的量的减少,应将洗涤液全部转移到容量瓶中,当溶液没冷却至室温时即定容,则冷却后溶液体积会偏小,影响浓度.
解答:
解:(1)配制250mL 1.25mol/L的NaOH溶液所需的氢氧化钠的质量m=c?V?M=1.25mol/L×0.25L×40g/mol=12.5g;根据容量瓶只有一条刻度线,只能配制与其规格相对应的体积的溶液,故配制250mL溶液,需要选用250mL容量瓶;操作步骤有计算、称量、溶解、移液、洗涤、定容、摇匀等操作,一般用托盘天平称量,用药匙取用药品,在烧杯中溶解(可用量筒量取水加入烧杯),并用玻璃棒搅拌,加速溶解.冷却后转移到250mL容量瓶中,并用玻璃棒引流,洗涤烧杯、玻璃棒2-3次,并将洗涤液移入容量瓶中,加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,最后定容颠倒摇匀.所以所需仪器有托盘天平、烧杯、玻璃棒、250mL容量瓶、胶头滴管.根据提供的仪器可知,还需仪器有托盘天平、玻璃棒、烧杯、胶头滴管.
故答案为:12.5;250;托盘天平、玻璃棒、烧杯、胶头滴管;
(2)容量瓶是用来配制一定体积、一定物质的量浓度溶液的定量容器,容量瓶上标有容量、刻度线,容量瓶只能在常温下使用,不能用来盛装过冷或过热的液体,不能用来稀释溶液或作为反应容器,还标有温度,故选①③⑤,
(3)根据配制步骤是计算、称量、溶解、冷却、移液、洗涤、定容、摇匀、装瓶可知正确的操作顺序是:B、C、A、F、E、D,故答案为:B、C、A、F、E、D;
(4)烧杯和玻璃棒上都沾有硫酸,洗涤液中含有少量的溶质,为避免溶质的量的减少,应将洗涤液全部转移到容量瓶中;溶液有热胀冷缩的性质,如果不冷却到室温,会导致溶液的体积偏小,配制溶液的浓度偏高.
故答案为:保证溶质全部转入容量瓶;容量瓶盛放热溶液时,体积不准.
故答案为:12.5;250;托盘天平、玻璃棒、烧杯、胶头滴管;
(2)容量瓶是用来配制一定体积、一定物质的量浓度溶液的定量容器,容量瓶上标有容量、刻度线,容量瓶只能在常温下使用,不能用来盛装过冷或过热的液体,不能用来稀释溶液或作为反应容器,还标有温度,故选①③⑤,
(3)根据配制步骤是计算、称量、溶解、冷却、移液、洗涤、定容、摇匀、装瓶可知正确的操作顺序是:B、C、A、F、E、D,故答案为:B、C、A、F、E、D;
(4)烧杯和玻璃棒上都沾有硫酸,洗涤液中含有少量的溶质,为避免溶质的量的减少,应将洗涤液全部转移到容量瓶中;溶液有热胀冷缩的性质,如果不冷却到室温,会导致溶液的体积偏小,配制溶液的浓度偏高.
故答案为:保证溶质全部转入容量瓶;容量瓶盛放热溶液时,体积不准.
点评:本题考查了一定物质的量浓度溶液的配制过程中的计算和误差分析,属于基础型题目,难度不大.

练习册系列答案
 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案
相关题目
对于可逆反应:4NH3(g)+5O2(g)?4NO(g)+6H2O(g),下列正确的是( )
A、平衡常数的表达式K=
| ||
| B、当v正(NH3):v正(NO)=1:1时,说明该反应已经达到平衡 | ||
| C、若平衡时两种反应物的转化率相等,则起始投入的n(NH3):n(O2)=5:4 | ||
| D、反应达到平衡后,恒容条件下,同倍数改变NH3和NO的量,c(O2)=可能不变 |
下列实验装置与实验操作正确的是( )
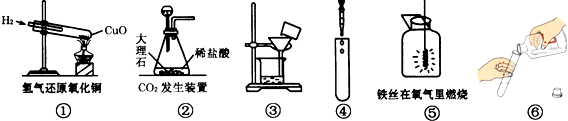

| A、①④⑥ | B、④⑥ |
| C、①②④⑤ | D、④⑤⑥ |
某混合气体G可能含有CO、CO2、SO2、H2O等气体,用a.无水CuSO4、b.澄清石灰水、c.灼热CuO、d.碱石灰、e.品红溶液、f.酸性高锰酸钾溶液等药品可将其一一检出,检出的正确顺序是…( )
| A、G→a→e→b→f→d→c |
| B、G→c→d→b→e→f→a |
| C、G→a→e→f→b→d→c |
| D、G→b→e→f→a→d→c |
向某盐溶液中滴加Ba(NO3)2溶液和过量的稀盐酸,有白色沉淀生成,则原溶液可能是( )
| A、KNO3溶液 |
| B、CaCl2溶液 |
| C、Na2SO4溶液 |
| D、Na2CO3溶液 |
 写出①、②、③、④的方程式.
写出①、②、③、④的方程式.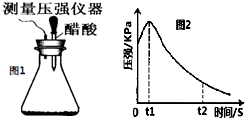 某研究小组为探究弱酸性条件下铁发生电化学腐蚀类型的影响因素,将混合均匀的新制铁粉和碳粉置于锥形瓶底部,塞上瓶塞(如图1).从胶头滴管中滴入几滴醋酸溶液,同时测量容器中的压强变化.
某研究小组为探究弱酸性条件下铁发生电化学腐蚀类型的影响因素,将混合均匀的新制铁粉和碳粉置于锥形瓶底部,塞上瓶塞(如图1).从胶头滴管中滴入几滴醋酸溶液,同时测量容器中的压强变化.
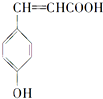 咖啡酸具有止血功效,存在于多种中药中,其结构简式为
咖啡酸具有止血功效,存在于多种中药中,其结构简式为