题目内容
对于可逆反应:4NH3(g)+5O2(g)?4NO(g)+6H2O(g),下列正确的是( )
A、平衡常数的表达式K=
| ||
| B、当v正(NH3):v正(NO)=1:1时,说明该反应已经达到平衡 | ||
| C、若平衡时两种反应物的转化率相等,则起始投入的n(NH3):n(O2)=5:4 | ||
| D、反应达到平衡后,恒容条件下,同倍数改变NH3和NO的量,c(O2)=可能不变 |
考点:化学平衡的影响因素
专题:化学平衡专题
分析:A.根据平衡常数的表达式进行判断;
B.v正(NH3):v正(NO)=1:1,只能说明正反应速率的关系;
C.达到平衡时,若两种反应物的转化率相等,则反应物的起始量之比等于化学计量数之比;
D.当反应达到平衡时,氨气和一氧化氮的浓度相等,故同倍数改变NH3和NO的量时浓度一直相等,根据K的表达式平衡常数保持不变,所以c(O2)=可能不变.
B.v正(NH3):v正(NO)=1:1,只能说明正反应速率的关系;
C.达到平衡时,若两种反应物的转化率相等,则反应物的起始量之比等于化学计量数之比;
D.当反应达到平衡时,氨气和一氧化氮的浓度相等,故同倍数改变NH3和NO的量时浓度一直相等,根据K的表达式平衡常数保持不变,所以c(O2)=可能不变.
解答:
解:A.平衡常数的表达式为K=
,故A错误;
B.v正(NH3):v正(NO)=1:1,只能说明正反应速率的关系,只有正逆反应相等可确定化学反应达到平衡,故B错误;
C.达到平衡时,若两种反应物的转化率相等,则反应物的起始量之比等于化学计量数之比,即起始投入的n (NH3 ):n (O2 )=4:5,故C错误;
D.当反应达到平衡时,氨气和一氧化氮的浓度相等,故同倍数改变NH3和NO的量时浓度一直相等,根据K的表达式平衡常数保持不变,所以c(O2)=可能不变,故D正确;
故选D.
| C(NO) 4C(H 2O) 6 |
| C(NH 3) 4C(O 2) 5 |
B.v正(NH3):v正(NO)=1:1,只能说明正反应速率的关系,只有正逆反应相等可确定化学反应达到平衡,故B错误;
C.达到平衡时,若两种反应物的转化率相等,则反应物的起始量之比等于化学计量数之比,即起始投入的n (NH3 ):n (O2 )=4:5,故C错误;
D.当反应达到平衡时,氨气和一氧化氮的浓度相等,故同倍数改变NH3和NO的量时浓度一直相等,根据K的表达式平衡常数保持不变,所以c(O2)=可能不变,故D正确;
故选D.
点评:本题考查化学平衡状态的判断、化学平衡移动的方向以及影响因素是现在考查的热点,注意知识的归纳和整理,难度不大.

练习册系列答案
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案
相关题目
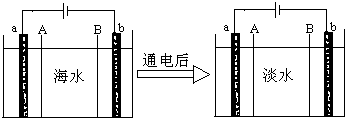 电渗析法将海水进行淡化,其原理如图.已知海水中含Na+、Cl-、Ca2+、Ba2+、SO42-等离子,电极为惰性电极.下列叙述中正确的是( )
电渗析法将海水进行淡化,其原理如图.已知海水中含Na+、Cl-、Ca2+、Ba2+、SO42-等离子,电极为惰性电极.下列叙述中正确的是( )| A、通电后,海水中阳离子往a电极处运动 |
| B、B膜是阴离子交换膜 |
| C、通电后,电子由b极经过溶液到达a极 |
| D、通电后,b电极上产生无色气体,溶液中少量白色沉淀 |
下列除去杂质的方法,正确的是( )
| A、除去乙烷中少量的乙烯:光照条件下通入Cl2,气液分离 |
| B、除去乙醇中少量乙酸:加入碳酸钠溶液,分液 |
| C、除去FeCl3溶液中少量的CuCl2:加入过量铁粉,过滤 |
| D、除去乙酸乙酯中少量的乙酸:用饱和碳酸钠溶液洗涤,分液 |
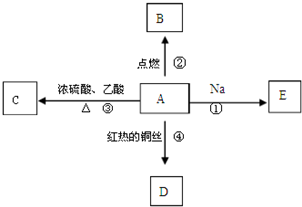 A是乙醇的同系物,其分子中只有1个甲基,相对分子质量为60,它能进行如图所示的多种反应:
A是乙醇的同系物,其分子中只有1个甲基,相对分子质量为60,它能进行如图所示的多种反应: