题目内容
2.蛇纹石矿可以看做由MgO、Fe2O3、Al2O3和SiO2组成.某实验小组设计如下流程欲分别制得单质Mg、Fe、Al和Si.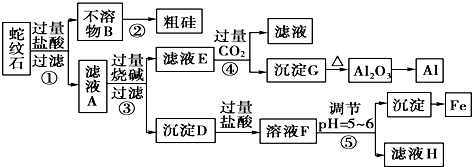
有关氢氧化物沉淀时的pH见如表:
| 金属阳离子 | 氢氧化物开始沉淀时的pH | 氢氧化物完全沉淀时的pH |
| Fe3+ | 1.9 | 3.2 |
| Mg2+ | 9.4 | 11.6 |
(1)滤液A中含有的阳离子有Fe3+、Al3+、Mg2+、H+;
(2)操作④中生成沉淀G的离子方程式为AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-;
(3)由G反应生成Al2O3的反应方程式2Al(OH)3$\frac{\underline{\;\;△\;\;}}{\;}$Al2O3+3H2O;
(4)操作⑤中调节pH=5~6时,可以用到的试剂为c(填字母).
a.NaOH溶液 b.氨水 c.MgO
(5)由滤液H制取金属Mg的流程如下:
滤液H$\stackrel{加热浓缩}{→}$$\stackrel{冷却结晶}{→}$MgCl2•6MgCl2-→Mg
该流程中由MgCl2冶炼Mg的方法是电解.
分析 蛇纹石矿加盐酸溶解,发生反应的化学方程式为MgO+2HCl=MgCl2+H2O,Fe2O3+6HCl=2FeCl3+3H2O,Al2O3+6HCl=2AlCl3+3H2O,SiO2不与盐酸反应,以固体形式先除去,因此,不溶物B为SiO2,滤液A中除了Mg2+外,还有的金属离子是Al3+和Fe3+,加入过量烧碱,滤液E为偏铝酸钠溶液,通入过量二氧化碳反应生成氢氧化铝沉淀,加热分解生成氧化铝,用电解法冶炼可生成铝;沉淀D为Fe(OH)3和Mg(OH)2,加入过量盐酸生成氯化铁和氯化铝,调节溶液pH=5~6时,促进铁离子水解,生成氢氧化铁沉淀,滤液H为氯化镁溶液,在HCl氛围中加热、蒸发结晶可得MgCl2•6H2O,脱水生成MgCl2,电解可得Mg,以此解答该题.
解答 解:(1)蛇纹石加过量盐酸溶解,MgO、Fe2O3、Al2O3和HCl反应溶解,反应方程式分别为:MgO+2HCl=MgCl2+H2O,Fe2O3+6HCl=2FeCl3+3H2O,Al2O3+6HCl=2AlCl3+3H2O.而SiO2不与盐酸反应,以沉淀的形式除去,所以滤液A中含有的阳离子有Fe3+、Al3+、Mg2+、H+,
故答案为:Fe3+、Al3+、Mg2+、H+;
(2)偏铝酸根离子和二氧化碳反应生成氢氧化铝和碳酸氢根离子,离子方程式为:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-,
故答案为:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-;
(3)氢氧化铝加入分解生成氧化铝,反应的方程式为2Al(OH)3$\frac{\underline{\;\;△\;\;}}{\;}$Al2O3+3H2O,故答案为:2Al(OH)3$\frac{\underline{\;\;△\;\;}}{\;}$Al2O3+3H2O;
(4)操作⑤中加入的物质能和盐酸反应,且不引进新的杂质,氧化镁、氢氧化镁难溶于水,但能与酸反应,可起调节pH作用,
故答案为:c;
(5)镁是活泼金属,应采用电解其熔融盐的方法冶炼,所以工业上用电解熔融氯化镁的方法冶炼镁,反应方程式为:MgCl2 $\frac{\underline{\;通电\;}}{\;}$ Mg+Cl2↑,
故答案为:电解.
点评 本题物质的制备,为高考常见题型,侧重于学生的分析能力和实验能力的考查,题目涉及元素化合物中金属铝、铁的性质,解题时不仅需熟知物质间的反应原理,还需灵活运用于实验的设计,题目难度中等.

 阅读快车系列答案
阅读快车系列答案| A. | 戊烷与乙烷 | B. | 淀粉和纤维素 | C. | 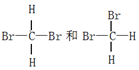 | D. | CH3CH2CH2CH3和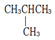 |
| A. | 加MgSO4 | B. | 加HCl溶液 | C. | 加NaOH | D. | 加少量水 |
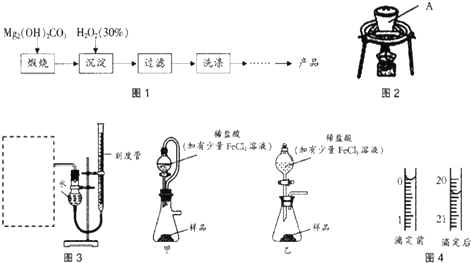
Ⅰ过氧化镁的制备
过氧化镁的制备流程如图1所示:
(1)用如图2所示装置进行煅烧,仪器A的名称是坩埚;
(2)某同学为了研究Mg2(OH)2CO3煅烧条件对合成MgO2的影响.设计实验如下表所示(所取固体质量均为ag),其他条件不变时,探究煅烧温度对合成MgO2的影响,可选择实验①③(填实验编号).
| 实验编号 | 煅烧温度(℃) | 煅烧时间(h) |
| ① | 550 | 2 |
| ② | 600 | 1 |
| ③ | 650 | 2 |
| ④ | 700 | 3 |
(3)某同学拟用图3装置测定一定质量的样品中过氧化镁的含量.
①图3装置中,虚线框内应选择装置甲(填“甲”或“乙”).②装置连接完毕后,进行气密性检验的方法为向量气管中加水到右端液面高出左端液面,若液面不发生变化,则气密性良好;③稀盐酸中加入少量FeCl3溶液作用是催化剂.
(4)某同学准确称取1.500g产品于锥形瓶中,加入15ml蒸馏水和15mL2.000mol•L-1 H2SO4,用0.5000mol•L-1KMnO4标准溶液滴定至终点.
反应的离子方程式为:2MnO4-+5H2O2+6H+═2Mn2++5O2↑+8H2O
①滴定终点观察到的现象为当滴入最后一滴高锰酸钾溶液后溶液由无色变为浅红色,且30s不褪色;
②根据图4计算产品中MgO2的质量分数为95.2%.
| A. | 能使淀粉-KI试纸显蓝色的溶液中:K+、H+、SO42-、I- | |
| B. | 能溶解CaCO3的溶液中:Fe2+、Ca2+、Cl-、NO3- | |
| C. | 在酸性KMnO4溶液中:Na+、C2H5OH、NH4+、Cl- | |
| D. | 澄清透明的溶液中:Cu2+、Mg2+、SO42-、Cl- |
| A. | 把金属铁放入稀硫酸中:Fe+2H+═Fe3++H2↑ | |
| B. | 往碳酸镁中滴加稀盐酸:CO32-+2H+═CO2↑+H2O | |
| C. | 氢氧化铜加到盐酸中:Cu(OH)2+2H+═Cu2++2H2O | |
| D. | 氢氧化钡溶液与稀硫酸反应:Ba2++SO42-+H++OH-═Ba SO4↓+H2O |
 如图所示,在大试管里加入3mL乙醇、2mL冰醋酸,再缓缓加入2mL浓硫酸,边加边振荡.在另一支试管中加入饱和碳酸钠溶液用来吸收反应生成物.
如图所示,在大试管里加入3mL乙醇、2mL冰醋酸,再缓缓加入2mL浓硫酸,边加边振荡.在另一支试管中加入饱和碳酸钠溶液用来吸收反应生成物.