题目内容
5.下列离子方程式中,正确的是( )| A. | 铜粉加入到Fe2(SO4)3溶液中:Cu+Fe3+═Cu2++Fe | |
| B. | 钠块投入到CuSO4溶液中:2Na+Cu2+═2Na++Cu↓ | |
| C. | Cl2通入到NaOH溶液中:Cl2+2OH-═Cl-+ClO-+H2O | |
| D. | 用NaOH溶液吸收少量CO2:OH-+CO2═HCO${\;}_{3}^{-}$ |
分析 A、电荷不守恒;
B、钠与水反应;
C、根据升降法配平;
D、少量二氧化碳生成碳酸根.
解答 解:A、电荷不守恒,故A错误;
B、钠与水反应,不能置换出铜单质,故B错误;
C、Cl2通入到NaOH溶液中的反应为:Cl2+2OH-═Cl-+ClO-+H2O,故C正确;
D、少量二氧化碳生成碳酸根,过量二氧化碳生成碳酸氢根,故D错误.
故选:C.
点评 本题考查学生有关离子反应的实质和离子方程式的书写知识,可以根据所学知识进行回答,难度不大.

练习册系列答案
相关题目
16.许多化学反应都伴随着明显而美丽的颜色变化,给学习和生活带来无穷乐趣,下列颜色变化中不属于化学变化的是( )
| A. | 新制氯水使有色布条褪色 | B. | 过氧化钠使某些燃料褪色 | ||
| C. | 二氧化硫使溴水褪色 | D. | 活性炭使红墨水褪色 |
13.下列说法中正确的是( )
| A. | sp3杂化轨道是由任意的1个s轨道和3个p轨道混合形成的四个sp3杂化轨道 | |
| B. | 乙炔分子中,每个碳原子都有两个未杂化的2p轨道形成π键 | |
| C. | 凡中心原子采取sp2杂化的分子,其分子构型都是平面三角形 | |
| D. | 凡AB2型的共价化合物,其中心原子A均采用sp杂化轨道成键 |
20.把X、Y、Z三种金属分别浸入相同质量分数的稀硫酸中,Y表面有气泡产生,X、Z表面无明显变化;把Z金属浸入X的硝酸盐溶液中,Z表面析出X.则三种金属的活动性顺序由强到弱的是( )
| A. | Y、Z、X | B. | X、Y、Z | C. | X、Z、Y | D. | Z、Y、X |
10.两种烃的衍生物A和B,所含碳、氢、氧的质量比均为6:1:4.完全燃烧0.1mol A能生成3.6g水.B只含一个醛基,1.1g B与足量银氨溶液反应,可析出2.7g Ag.则下列关于物质A和物质B的判断正确的是( )
| A. | 物质A一定是乙醛 | |
| B. | 物质B的分子式为C4H8O2 | |
| C. | 物质B的同分异构体中既含有醛基又含有羟基的共有6种 | |
| D. | 物质A和物质B互为同分异构体 |
14.漂白剂常用于日常生活和工业生产中,下列有关说法正确的是( )
| A. | 活性炭与新制氯水的漂白原理相同 | |
| B. | 过氧化钠常用于羽绒制品的漂白 | |
| C. | 漂白粉是由Ca(ClO)2组成的纯净物 | |
| D. | 将漂白剂SO2和NaClO混合使用可增加漂白效果 |
15.下列各元素原子半径依次增大的是( )
| A. | Na、Mg、Al | B. | Na、O、F | C. | P、Si、Al | D. | C、Si、P |
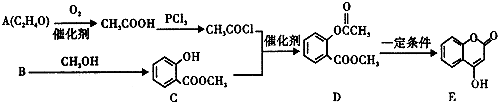
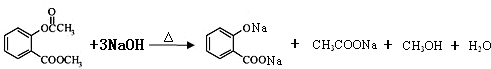 .
.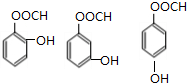 .
.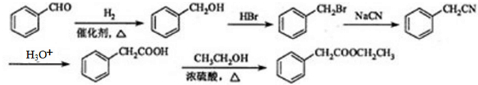 .
.