题目内容
20.下列化学用语中,书写错误的是( )| A. | 硫离子的结构示意图: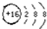 | B. | 氟化钠的电子式: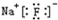 | ||
| C. | CaCl2的电子式: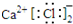 | D. | 次氯酸的结构式:H-Cl-O |
分析 A.硫离子的核电荷数为16,核外电子总数为18,最外层满足8电子稳定结构;
B.氟化钠为离子化合物,钠离子需要标出所带电荷,氟离子需要标出所带电荷及最外层电子;
C.氯化钙的电子式中,两个氯离子不能合并;
D.次氯酸的中心原子为氧原子,分子中不存在H-Cl键.
解答 解:A.硫离子的核电荷数为16,最外层达到8电子稳定结构,其离子结构示意图为: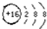 ,故A正确;
,故A正确;
B.氟化钠为离子化合物,阴阳离子需要标出所带电荷,其电子式为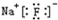 ,故B正确;
,故B正确;
C.氯化钙为离子化合物,电子式中需要标出阴阳离子所带电荷,氯化钙的电子式为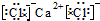 ,故C错误;
,故C错误;
D.次氯酸中含有1个H-O键和1个O-Cl键,其正确的结构式为:H-O-Cl,故D错误;
故选CD.
点评 本题考查了常见化学用语的表示方法,题目难度不大,涉及电子式、离子结构示意图、结构式等知识,明确常见化学用语的书写原则为解答关键,试题有利于培养学生的分析能力及规范答题能力.

练习册系列答案
相关题目
11.关于如图所示装置的叙述,正确的是( )


| A. | 此装置为原电池,铜片上有气泡产生 | |
| B. | 铜片质量逐渐减少 | |
| C. | 电流从锌片经导线流向铜片 | |
| D. | 氢离子在铜片表面被氧化 |
8. 过氧化氢(H2O2)被称为绿色氧化剂,其分子结构如图所示.两个氢原子位于不重合的两个平面上,而两个氧原子位于两平面的交线上.下列有关说法正确的是( )
过氧化氢(H2O2)被称为绿色氧化剂,其分子结构如图所示.两个氢原子位于不重合的两个平面上,而两个氧原子位于两平面的交线上.下列有关说法正确的是( )
 过氧化氢(H2O2)被称为绿色氧化剂,其分子结构如图所示.两个氢原子位于不重合的两个平面上,而两个氧原子位于两平面的交线上.下列有关说法正确的是( )
过氧化氢(H2O2)被称为绿色氧化剂,其分子结构如图所示.两个氢原子位于不重合的两个平面上,而两个氧原子位于两平面的交线上.下列有关说法正确的是( )| A. | 过氧化氢分子中含有H-H键、O-O键 | |
| B. | 过氧化氢分子中存在离子键和共价键 | |
| C. | 过氧化氢分子中只有共价键,其电子式为 | |
| D. | H2O2与H2O互为同位素 |
5.下列化学用语正确的是( )
| A. | 氟化氢的电子式: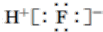 | B. | 中子数为21的钾原子:${\;}_{19}^{40}$K | ||
| C. | NH3的结构式: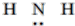 | D. | N3-的结构示意图: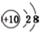 |
12.两种气态烃的混合物共1mol,在空气中完全燃烧生成2mol CO2气体和2.5mol水蒸气(气体体积均在相同状况下测定),关于该混合气体的说法正确的是( )
| A. | 一定含有乙烯 | |
| B. | 可能为等物质的量甲烷和丙烯的混合物 | |
| C. | 可能为乙烷和丙烷的混合物 | |
| D. | 一定为乙烯和甲烷的混合物 |
8.下列说法中不正确的是( )
| A. | 酸与醇反应一定能生成酯,且酯化反应是可逆反应 | |
| B. | CO2通入饱和苯酚钠溶液,用分液法可以得到苯酚 | |
| C. | 有机物 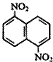 的n溴代物的同分异构体的数目与m溴代物的同分异构体的数目相等,则m、n一定满足的关系式m+n=6 的n溴代物的同分异构体的数目与m溴代物的同分异构体的数目相等,则m、n一定满足的关系式m+n=6 | |
| D. | 等物质的量的烃或烃的含氧衍生物A和B完全燃烧时,消耗氧气的量相等.则A和B的分子量相差可能为18n或44n(n为正整数) |
9.PCl3和PCl5都是重要的化工原料.将PCl3(g) 和Cl2(g)充入体积不变的2L密闭容器中,在一定条件下发生下述反应,并于10min时达到平衡:PCl3(g)+Cl2(g)?PCl5(g),有关数据如下:
下列判断不正确的是( )
| PCl3(g) | Cl2(g) | PCl5(g) | |
| 初始浓度(mol/L) | 2.0 | 1.0 | 0 |
| 平衡浓度(mol/L) | c1 | c2 | 0.4 |
| A. | 10 min内,v(Cl2)=0.04 mol/(L•min) | |
| B. | 当容器中Cl2为1.2 mol时,反应达到平衡 | |
| C. | 升高温度(T1<T2),反应的平衡常数减小,平衡时PCl3的$\frac{△n({T}_{1})}{△n({T}_{2})}$<1 | |
| D. | 平衡后移走2.0 mol PCl3和1.0 molCl2,在相同条件下再达平衡时,c(PCl5)<0.2 mol/L |

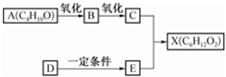 如图中X是无支链的、具有果香味的合成香料,可用于调配多种果香型香精.已知D在标准状况下的密度为1.25g•L-1,其产量可以用来衡量一个国家石油化工发展水平.E是生活中常见的一种有机物.各物质间转化关系如图:
如图中X是无支链的、具有果香味的合成香料,可用于调配多种果香型香精.已知D在标准状况下的密度为1.25g•L-1,其产量可以用来衡量一个国家石油化工发展水平.E是生活中常见的一种有机物.各物质间转化关系如图: .
.