题目内容
5.下列化学用语正确的是( )| A. | 氟化氢的电子式: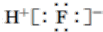 | B. | 中子数为21的钾原子:${\;}_{19}^{40}$K | ||
| C. | NH3的结构式: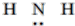 | D. | N3-的结构示意图: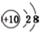 |
分析 A.氟化氢为共价化合物,分子中不存在阴阳离子;
B.质量数=质子数+中子数,元素符号的左上角为质量数、左下角为质子数;
C.结构式中需要用短线代替所有的共用电子对;
D.N3-的核电荷数应该为7.
解答 解:A.氟化氢中不存在阴阳离子,其电子式不能标出电荷,氟化氢正确的电子式为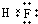 ,故A错误;
,故A错误;
B.中子数为21的钾原子的质量数为40,该原子可以表示为:${\;}_{19}^{40}$K,故B正确;
C.氨气分子中含有3个N-H键,其正确的结构式为: ,故C错误;
,故C错误;
D.N3-的核电荷数为7,核外电子总数为10,其正确的离子结构示意图为: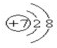 ,故D错误;
,故D错误;
故选B.
点评 本题考查了常见化学用语的表示方法,题目难度不大,涉及电子式、结构式、离子结构示意图、元素符号等知识,明确常见化学用语的书写原则为解答关键,试题培养了学生的分析能力及规范答题能力.

练习册系列答案
相关题目
16.依据下列甲、乙、丙三图,判断下列叙述不正确的是( )
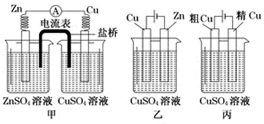

| A. | 甲是原电池,乙是电镀装置 | |
| B. | 甲、乙装置中,锌极上均发生氧化反应 | |
| C. | 乙、丙装置中,阳极均发生氧化反应而溶解 | |
| D. | 丙装置中,铜电极的质量有增有减 |
13.在一定条件下MO3-与M-发生反应;MO3-+5M-+6H+═3M2+3H2O,则下列关于M元素的叙述中正确的是( )
| A. | M的氢化物的水溶液呈酸性 | B. | M2在常温常压下一定是气体 | ||
| C. | MO3-中的M元素只能被还原 | D. | M位于元素周期表的第VA族 |
20.下列化学用语中,书写错误的是( )
| A. | 硫离子的结构示意图: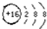 | B. | 氟化钠的电子式: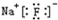 | ||
| C. | CaCl2的电子式: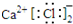 | D. | 次氯酸的结构式:H-Cl-O |
17.工业上用铝土矿(主要成分是Al2O3、SiO2、Fe2O3杂质)提取纯Al2O3再冶炼铝的过程如图所示,下列有关说法不正确的是( )


| A. | 实验室中灼烧操作通常在坩埚中进行 | |
| B. | 若X为烧碱,则Z为氨气,沉淀a为红棕色,可作颜料 | |
| C. | 若X为盐酸,则Z为CO2,溶液丙只含NaCl和Na2CO3 | |
| D. | 上述过程中所发生的反应有分解反应、复分解反应、氧化还原反应 |
13.常温下,下列有关溶液中微粒的物质的量浓度关系不正确的是( )
| A. | 向0.1mol/LpH=2的HF溶液加水稀释,$\frac{c({H}^{+})}{c(HF)}$增大 | |
| B. | 向0.2 mol/L NaHCO3溶液中加入等体积0.1 mol/L NaOH溶液c(HCO3-)>c(CO32-)>c(OH-)>c(H+) | |
| C. | 向0.1mol/L NaHSO3溶液中通入NH3至中性(溶液体积视为不变),则 c(NH4+)+c(H2SO3)═c(SO32-) | |
| D. | 现有常温下水电离出的c(H+)均为1×10-11 mol/L且体积相同的三种溶液:①HCl溶液②CH3COOH溶液③NaOH溶液,分别与足量铝粉反应,生成氢气的量③最少 |