题目内容
9.PCl3和PCl5都是重要的化工原料.将PCl3(g) 和Cl2(g)充入体积不变的2L密闭容器中,在一定条件下发生下述反应,并于10min时达到平衡:PCl3(g)+Cl2(g)?PCl5(g),有关数据如下:| PCl3(g) | Cl2(g) | PCl5(g) | |
| 初始浓度(mol/L) | 2.0 | 1.0 | 0 |
| 平衡浓度(mol/L) | c1 | c2 | 0.4 |
| A. | 10 min内,v(Cl2)=0.04 mol/(L•min) | |
| B. | 当容器中Cl2为1.2 mol时,反应达到平衡 | |
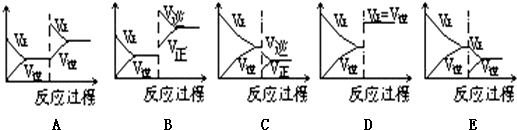
| C. | 升高温度(T1<T2),反应的平衡常数减小,平衡时PCl3的$\frac{△n({T}_{1})}{△n({T}_{2})}$<1 | |
| D. | 平衡后移走2.0 mol PCl3和1.0 molCl2,在相同条件下再达平衡时,c(PCl5)<0.2 mol/L |
分析 A.由表中数据可知,平衡时△c(PCl5)=0.4mol/L,根据方程式可知△c(PCl3)=0.4mol/L,根据v=$\frac{△c}{△t}$计算v(PCl3);
B.平衡时△c(PCl5)=0.4mol/L,根据方程式可知△c(Cl2)=0.4mol/L,根据△n=△c×V计算△n(Cl2),进而计算平衡时Cl2的物质的量;
C.升高温度,反应的平衡常数减小,平衡向逆反应移动;
D、平衡后移走2.0mol PCl3和1.0mol Cl2到达的平衡,等效为开始PCl3为1mol/L、Cl2为0.5mol/L到达平衡,与原平衡相比,压强降低,平衡向逆反应移动,反应物转化率降低.
解答 解:A.由表中数据可知,平衡时△c(PCl5)=0.4mol/L,根据方程式可知△c(PCl3)=0.4mol/L,v(PCl3)=$\frac{0.4mol/L}{10min}$=0.04mol•L-1•min-1,故A正确;
B.平衡时△c(PCl5)=0.4mol/L,根据方程式可知△c(Cl2)=0.4mol/L,△n(Cl2)=0.4mol/L×2L=0.8mol,故平衡时Cl2的物质的量为1mol/L×2L-0.8mol=1.2mol,故B正确;
C.升高温度,反应的平衡常数减小,平衡向逆反应移动,PCl3转化率降低,△n减小,故平衡时PCl3的$\frac{△n({T}_{1})}{△n({T}_{2})}$>1,故C错误;
D、平衡后移走2.0mol PCl3和1.0mol Cl2到达的平衡,等效为开始PCl3为1mol/L、Cl2为0.5mol/L到达平衡,反应物的浓度变为原平衡的一半,与原平衡相比,压强降低,平衡向逆反应移动,反应物转化率降低,故相同条件下再达平衡时,c(PCl5)<0.2 mol•L-1,故D正确;
故选C.
点评 本题考查化学平衡常数的应用、化学平衡的有关计算等,难度中等,注意D选项中构建平衡建立的途径.

| A. | 硫离子的结构示意图: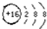 | B. | 氟化钠的电子式: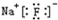 | ||
| C. | CaCl2的电子式: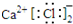 | D. | 次氯酸的结构式:H-Cl-O |
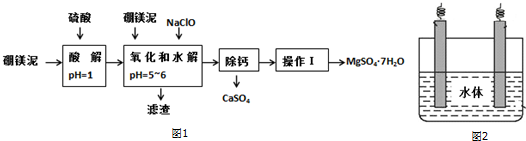
已知:某些氢氧化物沉淀的pH如下表所示.
| 氢氧化物 | 开始沉淀时的pH | 完全沉淀时的pH |
| Mg(OH)2 | 9.3 | 10.8 |
| Fe(OH)2 | 7.6 | 9.6 |
| Fe(OH)3 | 2.7 | 3.7 |
| Al(OH)3 | 3.7 | 4.7 |
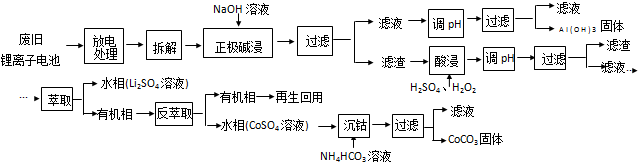
(1)在酸解过程中,欲加快酸解时的化学反应速率,请提出两种可行的措施:适当升温、把硼镁泥粉碎、或搅拌、或适当增加硫酸浓度.
(2)加入的NaClO可与Mn2+反应:Mn2++ClO-+H2O=MnO2↓+2H++Cl-,还有一种离子也会被NaClO氧化,并发生水解,该反应的离子方程式为2Fe2++ClO-+5H2O=2Fe(OH)3↓+Cl-+4H+.
(3)滤渣的主要成份除含有Fe(OH)3、Al(OH)3、MnO2外,还有SiO2、CaSO4.
(4)已知MgSO4、CaSO4的溶解度如下表:
| 温度(℃) | 40 | 50 | 60 | 70 |
| MgSO4 | 30.9 | 33.4 | 35.6 | 36.9 |
| CaSO4 | 0.210 | 0.207 | 0.201 | 0.193 |
(5)实验中提供的硼镁泥共100g,得到的MgSO4•7H2O为172.2g,计算MgSO4•7H2O的产率为70%.(保留两位有效数字)
(6)金属镁可用于自然水体中铁件的电化学防腐,完成图2防腐示意图,并作相应标注.
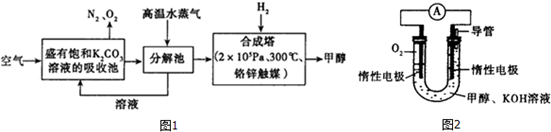
(1)向分解池中通入高温水蒸气的作用是提供高温环境使KHCO3分解.
(2)已知在常温常压下:①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)△H=-1275.6kJ•mol-1
②2CO(g)+O2(g)=2CO2(g)△H=-566.0kJ•mol-1
③H2O(g)=H2O(l)△H=-44.0kJ•mol-1
则甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为CH3OH(l)+O2(g)=CO (g)+2H2O(l)△H=-442.8KJ/mol.
(3)依据甲醇燃烧的反应原理.设计如图2所示的电池装置.该装置负极的电极反应式为CH3OH+8OH--6e-=CO32-+6H2O.
(4)已知Ksp(CaCO3)=2.8×10-9mol2•L-2.现将CaCl2溶液与0.02mol•L-1Na2CO3溶液等体积混合,生成CaCO3沉淀时,所需CaCl2溶液的最小物质的量浓度为5.6×10-7mol/L.
(5)CO(g)和H2O(g)在一定条件下反应可得到清洁燃料H2.将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中发生反应:CO(g)+H2O(g)?CO2(g)+H2(g),不同温度下得到三组数据:
| 实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需要的时间/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
②实验2条件下平衡常数K=0.17.
③该反应的△H<0 (填“<”或“>”=).
| A. | 只含有一种元素的物质 | B. | 漂粉精 | ||
| C. | 只含有一种分子式的物质 | D. | 胆矾 |
①MgCl2②Ba(NO3)2③K2SO4④CH4⑤KOH ⑥H2O.
| A. | ①②⑥ | B. | ③④⑥ | C. | ②③⑤ | D. | ①④⑤ |