题目内容
 如图的曲线是800℃时,A、B、C三种气体物质的浓度随时间变化的情况,t是平衡的时间,能以此曲线表示的反应是( )
如图的曲线是800℃时,A、B、C三种气体物质的浓度随时间变化的情况,t是平衡的时间,能以此曲线表示的反应是( )| A、2A?B+3C |
| B、B+3C?2A |
| C、A+C?B |
| D、B?A+C |
考点:物质的量或浓度随时间的变化曲线
专题:化学平衡专题
分析:根据反应物减少,生成物增加,变化的物质的量浓度之比等于反应中计量数之比,写出化学方程式,A的起始量为2,B、C的起始量均为0,说明A为反应物,B、C为生成物,达到平衡后,A、C的量为1.2,B的量为0.4,即A、B、C的变化量分别为0.8、0.4、1.2,根据物质的变化量之比等于物质的化学计量数之比,可得反应方程式为2A?B+3C.
解答:
解:A的起始量为2,B、C的起始量均为0,说明A为反应物,B、C为生成物,达到平衡后,A、C的量为1.2,B的量为0.4,即A、B、C的变化量分别为0.8、0.4、1.2,根据物质的变化量之比等于物质的化学计量数之比,可得反应方程式为2A?B+3C,故选:A.
点评:本题主要考查了根据图象写化学方程式,难度不大,是对基础知识的考查,解题时注意正确理解图象的内容即可.

练习册系列答案
相关题目
混合下列各组物质使之充分反应,加热蒸干产物并在300℃灼烧至质量不变,最终残留固体为纯净物的是( )
| A、向CuSO4溶液中加入适量铁粉 |
| B、等物质的量浓度、等体积的Na2SO4与BaCl2溶液 |
| C、等物质的量的NaHCO3与Na2O2固体 |
| D、在NaBr溶液中通入过量氯气 |
下列各反应属于加成反应的是( )
A、CH4+2O2
| ||
| B、CH2═CH2+Br2→CH2Br-CH2Br | ||
| C、CH4+Cl2→CH3Cl+HCl | ||
| D、2CH3CH2OH+O2→2CH3CHO+2H2O |
已知:C+CO2?2CO,正反应为吸热反应,达到平衡后,改变下列条件,能使平衡常数增大的是( )
| A、升温 | B、加压 |
| C、降温 | D、使用催化剂 |
自然界里常见金属元素存在最多的是铝,其次是铁,铜的含量较少.然而人类冶炼金属获得成功最早的反而是含量少的铜,含量最多的铝最迟冶炼出来,究其原因,合理的是( )
| A、铜矿较易还原,铝矿很难还原 |
| B、铜矿颜色较深,易发现;铝矿颜色较浅,不易发现 |
| C、矿石在地下埋藏,铜矿最浅,容易开发,铝矿埋得深,难开发 |
| D、以上说法都是错误的 |
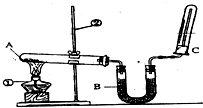 某同学为了探究氯化铵的性质,进行了如下实验,请你按要求回答下列问题:
某同学为了探究氯化铵的性质,进行了如下实验,请你按要求回答下列问题: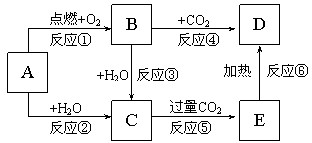 如图所示,A为一种常见的单质,B、C、D、E是含A元素的常见化合物,它们的焰色反应均为黄色.
如图所示,A为一种常见的单质,B、C、D、E是含A元素的常见化合物,它们的焰色反应均为黄色.