题目内容
14.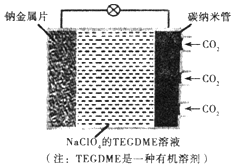 我国对可呼吸的钠-二氧化碳电池的研究取得突破性进展,该电池的总反应式为:4Na+3CO2$?_{充电}^{放电}$2Na2CO2+C,其工作原理如图所示(放电时产生的碳酸钠固体储存于碳纳米管中).关于该电池,下列说法错误的是( )
我国对可呼吸的钠-二氧化碳电池的研究取得突破性进展,该电池的总反应式为:4Na+3CO2$?_{充电}^{放电}$2Na2CO2+C,其工作原理如图所示(放电时产生的碳酸钠固体储存于碳纳米管中).关于该电池,下列说法错误的是( )| A. | 充电时,Na+从阳极向阴极移动 | |
| B. | 可以用乙醇代替TEGDME做有机溶剂 | |
| C. | 放电时,当转移lmol电子负极质量减轻23g | |
| D. | 放电时,正极反应为3CO2+4Na++4e-=2Na2CO3+C |
分析 由4Na+3CO2 $?_{充电}^{放电}$2Na2CO3+C可知,放电为原电池反应,Na为负极失去电子,正极上C得到电子;充电为电解池,阳极与正极相连,阳极失去电子发生氧化反应,电解时阳离子向阴极移动,以此来解答.
解答 解:A.充电为电解池,Na+从阳极向阴极移动,故A正确;
B.钠与乙醇反应,不能用乙醇代替TEGDME做有机溶剂,故B错误;
C.放电时负极发生Na-e-=Na+,转移lmol电子负极质量减轻23g,故C正确;
D.阳极反应为C+2Na2CO3-4e-=3CO2↑+4Na+,放电时正极反应为3CO2+4Na++4e-=2Na2CO3+C,故D正确;
故选B.
点评 本题考查原电池及电解池,为高频考点,把握电极判断、电极反应、工作原理为解答的关键,侧重分析与应用能力的考查,注意电化学知识的应用及钠的性质,题目难度不大.

练习册系列答案
相关题目
20.在元素周期表中,在金属元素与非金属元素的分界线附近可以找到( )
| A. | 作为催化剂的材料 | B. | 电子工业上的半导体材料 | ||
| C. | 制造农药的材料 | D. | 制造耐高温材料 |
5.如表是元素周期表的一部分,表中所列的字母分别代表某一化学元素
(1)表中所列元素中属于主族元素的有a、b、c、d、f、g、h、i、j、k、l;属于金属元素的有b、c、d、e、f、h;e在元素周期表中的位置是第四周期 VIII族.
(2)下列AC组元素的单质可能都是电的良导体.
A.d、e、f B.b、c、i C.c、d、g D.a、g、k
(3)表中某元素的最高价氧化物对应水化物呈两性的化学式是Al(OH)3,
它与短周期元素b的最高价氧化物对应水化物发生反应的离子方程式是Al(OH)3+OH-=AlO2-+2H2O;
(4)b、a与j形成原子个数比为1:1:1的化合物中含有的化学键类型是离子键和共价键.
| a | ||||||||||||||||||
| g | j | |||||||||||||||||
| b | c | f | i | l | m | |||||||||||||
| e | h | k | ||||||||||||||||
(2)下列AC组元素的单质可能都是电的良导体.
A.d、e、f B.b、c、i C.c、d、g D.a、g、k
(3)表中某元素的最高价氧化物对应水化物呈两性的化学式是Al(OH)3,
它与短周期元素b的最高价氧化物对应水化物发生反应的离子方程式是Al(OH)3+OH-=AlO2-+2H2O;
(4)b、a与j形成原子个数比为1:1:1的化合物中含有的化学键类型是离子键和共价键.
2.某学生探究0.25mol/LAl2(SO4)3溶液与0.5mol/LNa2CO3溶液的反应,实验如表.
下列分析不正确的是( )
| 实验1 | 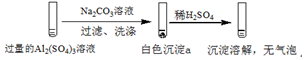 |
| 实验2 | 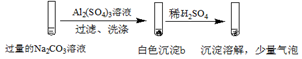 |
| A. | 实验1中,白色沉淀a是Al(OH)3 | |
| B. | 实验2中,白色沉淀b含有CO32- | |
| C. | 实验1、2中,白色沉淀成分不同的原因与混合后溶液的pH无关 | |
| D. | 检验白色沉淀a、b是否洗涤干净,均可用盐酸酸化的BaCl2溶液 |
9.下列实验操作、实验现象及对应的实验结论都正确的一组是( )
| 选项 | 实验操作 | 实验现象 | 实验结论 |
| A | 将CO2通入CaCl2溶液中 | 产生白色沉淀 | CaCO3难溶于水 |
| B | 向某溶液滴加少量稀盐酸 | 溶液中出现白色沉淀 | 该溶液中一定存在Ag+ |
| C | 向AgCl沉淀中滴加NaBr溶液 | 白色沉淀转化为浅黄色沉淀 | Ksp(AgCl)>Ksp(AgBr) |
| D | 将苯滴加到溴水中 | 溴水褪色 | 苯和溴发生了取代反应 |
| A. | A | B. | B | C. | C | D. | D |
19.下列关于实验室制取乙酸丁酯的叙述,正确的是( )
| A. | 使用过量的乙酸 | B. | 采用边反应边蒸馏的方法 | ||
| C. | 反应采用水浴加热 | D. | 用氢氧化钠溶液提纯乙酸丁酯 |
6.下列反应的离子方程式书写正确的是( )
| A. | 铁粉与稀H2SO4反应:2Fe+6H+═2Fe3++3H2↑ | |
| B. | Na2CO3溶液与足量盐酸反应:CO32-+2H+═CO2↑+H2O | |
| C. | Cu(OH)2固体与稀硫酸反应:OH-+H+═H2O | |
| D. | 铝片与NaOH溶液反应:Al+OH-+H2O═AlO2-+H2↑ |
3. X、Y、Z、M、Q、R皆为前20号元素,其原子半径与主要化合价的关系如图所示.下列说法错误的是( )
X、Y、Z、M、Q、R皆为前20号元素,其原子半径与主要化合价的关系如图所示.下列说法错误的是( )
 X、Y、Z、M、Q、R皆为前20号元素,其原子半径与主要化合价的关系如图所示.下列说法错误的是( )
X、Y、Z、M、Q、R皆为前20号元素,其原子半径与主要化合价的关系如图所示.下列说法错误的是( )| A. | Z与M的最高价氧化物对应水化物均为强酸 | |
| B. | X、Y、Z三种元素组成的化合物可能是酸、碱或盐 | |
| C. | 简单离子半径:M>Y>Q | |
| D. | 电解RM2水溶液可得到R单质 |
4.下列装置不能达到除杂目的(括号内为杂质)的是( )
| A. |  乙烷(乙烯) | B. |  苯(甲苯) | C. | 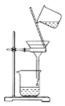 溴苯(CaO) | D. |  I2(CCl4) |