题目内容
为防止药品变质,实验室通常采用密封的方法保存.少量的金属钠存放在盛有煤油的广口瓶中而不是直接存放在密封的广口瓶中
(1)请解释原因:
(2)若金属钠直接露置在空气中,有下列现象①变成白色粉末②变暗③变成白色固体④固体表面变潮湿.上述现象出现的先后顺序是 .
(1)请解释原因:
(2)若金属钠直接露置在空气中,有下列现象①变成白色粉末②变暗③变成白色固体④固体表面变潮湿.上述现象出现的先后顺序是
考点:化学试剂的存放,钠的化学性质
专题:
分析:钠是活泼的金属,易和水、氧气反应,钠的密度大于煤油的密度,所以要保存钠应该隔绝空气和水蒸气,据此分析解答.
解答:
解:(1)钠和空气中氧气和水蒸气都反应,所以不能保存在广口瓶中;钠的密度小于煤油的密度,且和煤油不反应,所以钠可以保存在煤油中而隔绝空气和水;
故答案为:钠和空气中氧气和水蒸气都反应,所以不能保存在广口瓶中,且钠的密度小于煤油的密度,且和煤油不反应,所以钠可以保存在煤油中而隔绝空气和水;
(2)若金属钠直接露置在空气中,钠容易和氧气发生缓慢氧化生成Na2O(变暗),Na2O吸收空气中的水分生成NaOH(变成白色固体),NaOH又具有吸湿性,反应生成的NaOH表面潮解会变成NaOH溶液(固体表面变潮湿),最终NaOH与空气中的CO2生成Na2CO3(白色粉末),
故答案为:②③④①.
故答案为:钠和空气中氧气和水蒸气都反应,所以不能保存在广口瓶中,且钠的密度小于煤油的密度,且和煤油不反应,所以钠可以保存在煤油中而隔绝空气和水;
(2)若金属钠直接露置在空气中,钠容易和氧气发生缓慢氧化生成Na2O(变暗),Na2O吸收空气中的水分生成NaOH(变成白色固体),NaOH又具有吸湿性,反应生成的NaOH表面潮解会变成NaOH溶液(固体表面变潮湿),最终NaOH与空气中的CO2生成Na2CO3(白色粉末),
故答案为:②③④①.
点评:本题考查了钠的性质,根据钠的物理性质和化学性质来分析解答即可,难度不大.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案
相关题目
某芳香烃A(分子式为C9H10,含有一个碳碳双键)有如下转化关系: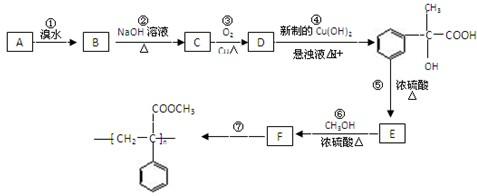
按要求填空:
(1)写出反应①的反应类型 ;反应⑤的反应类型 ;
(2)写出A和F结构简式:A ;F ;
(3)写出反应③的化学方程式: .

按要求填空:
(1)写出反应①的反应类型
(2)写出A和F结构简式:A
(3)写出反应③的化学方程式:
将浓度为0.1mol?L-1HF溶液加水不断稀释,下列各量始终保持增大的是( )
| A、c(H+) | ||
| B、K(HF) | ||
C、
| ||
D、
|
下列说法正确的是( )
| A、煤是复杂的混合物,含有苯、甲苯、二甲苯等一系列重要的化工原料 |
| B、石油分馏得到的汽油、煤油、柴油等都有固定的熔沸点 |
| C、石油炼制的目的是为了获得轻质油和重要化工原料(乙烯、丙烯等) |
| D、电解冶炼铝的原料是氯化铝 |
工业上由二氧化锰制备高锰酸钾可分二步进行,第一步:二氧化锰与氢氧化钾共熔并通入氧气2MnO2+4KOH+O2
2K2MnO4+2H2O;第二步:电解锰酸钾溶液:2K2MnO4+2H2O
2KMnO4+H2↑+2KOH则下列说法正确的是( )
| ||
| ||
| A、根据上述过程,每生成1molKMnO4,共转移6mol电子 | ||||
B、第二步电解时,阳极电极反应式为2MnO
| ||||
C、第二步电解的离子方程式为:2H2O
| ||||
| D、第二步电解时阴极周围pH减小 |
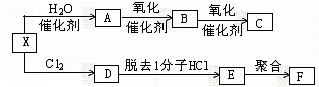
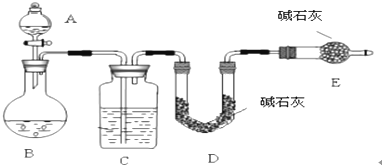
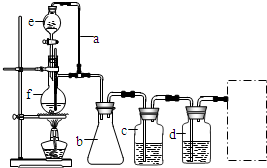 某研究性学习小组为合成1-丁醇,查阅资料得知一条合成路线:CH3CH=CH2+CO+H2
某研究性学习小组为合成1-丁醇,查阅资料得知一条合成路线:CH3CH=CH2+CO+H2