题目内容
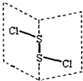 二氯化硫(S2Cl2)广泛用于橡胶工业,分子结构如图.常温下,S2Cl2是一种橙黄色液体,与水迅速反应,并生成能使品红褪色的气体.下列说法正确的是( )
二氯化硫(S2Cl2)广泛用于橡胶工业,分子结构如图.常温下,S2Cl2是一种橙黄色液体,与水迅速反应,并生成能使品红褪色的气体.下列说法正确的是( )A、S2Cl2的电子式: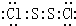 |
| B、S2Cl2为含有极性键和非极性键的非极性分子 |
| C、S2Br2与S2Cl2结构相似,熔沸点:S2Br2<S2Cl2 |
| D、S2Cl2与H2O反应化学方程式可能为:2 S2Cl2+2H2O=SO2↑+3S↓+4HCl |
考点:含硫物质的性质及综合应用
专题:
分析:A.由结构可知,S2Cl2分子中S原子之间形成1对共用电子对,Cl原子与S原子之间形成1对共用电子对,S应满足8电子稳定结构;
B.同种元素原子之间形成非极性键,不同元素的原子之间形成的化学键多为极性键;S2Cl2是展开书页型结构,Cl-S位于两个书页面内,该物质结构不对称;
C.相对分子质量越大,分子间作用力越大,熔沸点越高;
D.S2Cl2遇水易水解,并产生能使品红溶液褪色的气体,该气体为二氧化硫,在反应过程中硫元素一部分升高到+4价(生成SO2),一部分降低到0价(生成S),符合氧化还原反应原理.
B.同种元素原子之间形成非极性键,不同元素的原子之间形成的化学键多为极性键;S2Cl2是展开书页型结构,Cl-S位于两个书页面内,该物质结构不对称;
C.相对分子质量越大,分子间作用力越大,熔沸点越高;
D.S2Cl2遇水易水解,并产生能使品红溶液褪色的气体,该气体为二氧化硫,在反应过程中硫元素一部分升高到+4价(生成SO2),一部分降低到0价(生成S),符合氧化还原反应原理.
解答:
解:A.由结构可知,S2Cl2分子中S原子之间形成1对共用电子对,Cl原子与S原子之间形成1对共用电子对,S2Cl2的电子式为  ,故A错误;
,故A错误;
B.S2Cl2分子中S-S为非极性键,S-Cl键为极性键,S2Cl2是展开书页型结构,Cl-S位于两个书页面内,该物质结构不对称,正负电荷重心不重合,为极性分子,故B错误;C.S2Br2与S2Cl2结构相似,相对分子质量S2Br2>S2Cl2,则分子间作用力S2Br2>S2Cl2,故C错误;
D.S2Cl2遇水易水解,并产生能使品红溶液褪色的气体,该气体为二氧化硫,在反应过程中硫元素一部分升高到+4价(生成SO2),一部分降低到0价(生成S),符合氧化还原反应原理,即水解反应为2S2Cl2+2H2O=SO2↑+3S↓+4HCl,故D正确.
故选D.
 ,故A错误;
,故A错误;B.S2Cl2分子中S-S为非极性键,S-Cl键为极性键,S2Cl2是展开书页型结构,Cl-S位于两个书页面内,该物质结构不对称,正负电荷重心不重合,为极性分子,故B错误;C.S2Br2与S2Cl2结构相似,相对分子质量S2Br2>S2Cl2,则分子间作用力S2Br2>S2Cl2,故C错误;
D.S2Cl2遇水易水解,并产生能使品红溶液褪色的气体,该气体为二氧化硫,在反应过程中硫元素一部分升高到+4价(生成SO2),一部分降低到0价(生成S),符合氧化还原反应原理,即水解反应为2S2Cl2+2H2O=SO2↑+3S↓+4HCl,故D正确.
故选D.
点评:本题以S2Cl2的结构为载体,考查分子结构、化学键、电子式、氧化还原反应等,题目难度中等,是对基础知识的综合运用与学生能力的考查,注意基础知识的全面掌握,是一道不错的能力考查题目.注意利用信息中物质的结构结合所学知识来解答.

练习册系列答案
相关题目
将浓度为0.1mol?L-1HF溶液加水不断稀释,下列各量始终保持增大的是( )
| A、c(H+) | ||
| B、K(HF) | ||
C、
| ||
D、
|
下列条件下的水溶液中,离子一定能大量共存或符合该水溶液条件的是( )
| A、无色溶液中:K+、H+、SO42-、MnO4- |
| B、c(H+):c(OH-)=10-10的溶液中:K+、Na+、CO32-、AlO2- |
| C、c(H+):c(OH-)=1溶液中:K+、Na+、NO3-、ClO- |
| D、能使pH试纸变蓝色的溶液中:Ca2+、Na+、CO32-、SO42- |
下列关于有机物的叙述正确的是( )
| A、所有烷烃和糖类中都存在碳碳单键 |
| B、丁烷有两种同分异构体 |
| C、甲烷与氯气混合光照后黄绿色消失,是因为发生了加成反应 |
| D、向蛋白质溶液中加入饱和食盐水,蛋白质析出,加水也不溶解 |
以下结构简式表示一种有机物的结构,关于其性质的叙述不正确的是( )
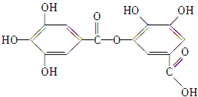

| A、它有酸性,能与纯碱溶液反应 |
| B、可以水解,其水解产物只有一种 |
| C、1 mol该有机物最多能与7 mol NaOH反应 |
| D、该有机物能发生取代反应 |
工业上由二氧化锰制备高锰酸钾可分二步进行,第一步:二氧化锰与氢氧化钾共熔并通入氧气2MnO2+4KOH+O2
2K2MnO4+2H2O;第二步:电解锰酸钾溶液:2K2MnO4+2H2O
2KMnO4+H2↑+2KOH则下列说法正确的是( )
| ||
| ||
| A、根据上述过程,每生成1molKMnO4,共转移6mol电子 | ||||
B、第二步电解时,阳极电极反应式为2MnO
| ||||
C、第二步电解的离子方程式为:2H2O
| ||||
| D、第二步电解时阴极周围pH减小 |
下列关于催化剂的说法,正确的是( )
| A、催化剂能使不起反应的物质发生反应 |
| B、在化学反应前后催化剂性质和质量都发生改变 |
| C、催化剂能改变化学反应速率 |
| D、在化学反应过程中,一定不参与化学反应 |