题目内容
15.把下列现象中硫酸所表现出来的性质填写在空白处(如:酸性、强氧化性、脱水性、吸水性).(1)用稀硫酸清洗铁锈,有气体放出.酸性
(2)盛有浓硫酸的烧杯敞口放置一段时间后,质量增加.吸水性
(3)用玻璃棒蘸浓硫酸滴在纸上时,纸变黑.脱水性
(4)把木炭放入热的浓硫酸中时,有气体放出.强氧化性
(5)在常温下可以用铁、铝制容器盛装冷的浓硫酸.强氧化性.
分析 硫酸具有强酸性,可用于制备氢气;具有吸水性,可用作干燥剂;具有吸水性,可使碳氢氧组成的有机物碳化,具有强氧化性,可使铝、铁钝化,在加热条件下与碳发生氧化还原反应,
(1)用稀硫酸清洗铁锈,有气体放出是氧化铁溶于稀硫酸后,铁和稀硫酸发生反应生成氢气;
(2)浓硫酸具有吸水性,能吸收水分而作干燥剂;
(3)浓硫酸能将有机物中的H、O元素以水分子形式脱去;
(4)把木炭放入热的浓硫酸中时生成二氧化碳、二氧化硫和水;
(5)常温下,浓硫酸和铁、铝发生钝化现象..
解答 解:(1)用稀硫酸清洗铁锈,有气体放出,是稀硫酸和铁反应生成了氢气,表现了硫酸的酸性,故答案为:酸性;
(2)浓硫酸具有吸水性,能吸收空气中的水蒸气,所以盛有浓硫酸的烧杯敞口放置一段时间后因为吸收空气中的水蒸气而导致质量增加,故答案为:吸水性;
(3)浓硫酸将纸张中的H、O元素以2:1水分子的形式脱去,体现脱水性,故答案为:脱水性;
(4)把木炭放入热的浓硫酸中时生成二氧化碳、二氧化硫和水,体现的是浓硫酸的强氧化性,故答案为:强氧化性;
(5)工业上用铁槽车或铝槽车运输浓硫酸,利用了浓硫酸的强氧化性,与铝、铁在常温下发生钝化反应,故答案为:强氧化性;
点评 本题综合考查浓硫酸的性质,为高考常见题型和高频考点,注意浓硫酸的特性,学习中注意相关基础知识的积累,难度不大.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案
相关题目
5.对于${\;}_{1}^{1}$H和${\;}_{1}^{2}$H+两种粒子,下列叙述正确的是( )
| A. | 质子数一定相同,质量数和中子数一定不同 | |
| B. | 化学性质几乎完全相同 | |
| C. | 一定都由质子、中子、电子构成 | |
| D. | 核电荷数,核外电子数一定相同 |
6.下列各烧杯中盛有海水,铁在其中发生腐蚀最慢的是( )
| A. | 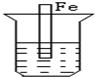 | B. |  | C. | 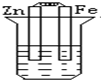 | D. | 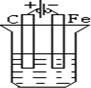 |
10.下列反应的离子方程正确的是( )
| A. | 钠与水反应:Na+2H2O═Na++2OH-+H2↑ | |
| B. | 碳酸钠溶液中加入足量盐酸:CO32-+2H+═CO2↑+H2O | |
| C. | 铁与稀盐酸反应:2Fe+6H+═2Fe3++3H2↑ | |
| D. | 氯化铝溶液中加入过量的氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O |
20.80mL稀硫酸与足量氯化钡溶液反应,得到46.6g沉淀,此稀硫酸的浓度是( )
| A. | 5mol/L | B. | 1.25mol/L | C. | 2.5mol/L | D. | 3mol/L |
4.下列有关燃料电池的说法正确的是( )
| A. | 氢氧燃料电池可将热能直接转变为电能 | |
| B. | 燃料电池的能量转化率可达100% | |
| C. | 燃料电池与干电池或蓄电池的主要差别在于反应物不是储存在电池内部,而是由外设装备提供燃料和氧化剂 | |
| D. | 氢氧燃料电池工作时氢气在正极被氧化 |
5.下列说法正确的是( )
| A. | 石油化工水平的标志是乙烯产量 | |
| B. | 天然气的主要成分是丙烷 | |
| C. | 糖尿病患者不可以用新制备的氢氧化铜检验 | |
| D. | 乙醇在铜丝的催化氧化下可生成无色无刺激性的乙醛 |
