题目内容
5.下列说法正确的是( )| A. | 石油化工水平的标志是乙烯产量 | |
| B. | 天然气的主要成分是丙烷 | |
| C. | 糖尿病患者不可以用新制备的氢氧化铜检验 | |
| D. | 乙醇在铜丝的催化氧化下可生成无色无刺激性的乙醛 |
分析 A.乙烯的产量是衡量石油化工水平的标志;
B.天然气的主要成分为甲烷;
C.葡萄糖可与氢氧化铜浊液发生氧化还原反应;
D.乙醛有刺激性气味.
解答 解:A.乙烯具有广泛的工业用途,其产量是衡量石油化工水平的标志,故A正确;
B.天然气的主要成分为甲烷,故B错误;
C.糖尿病患者尿液中葡萄糖含量较高,葡萄糖可与氢氧化铜浊液发生氧化还原反应,故C错误;
D.乙醛有刺激性气味,故D错误.
故选A.
点评 本题考查较为综合,为高考常见题型,侧重于化学与生活的考查,有利于培养学生良好的科学素养,提高学习的积极性,难度不大,注意相关基础知识的积累.

练习册系列答案
相关题目
16.元素单质及其化合物有广泛用途,对于元素周期表中第3周期的元素来说,按原子序数递增的顺序(稀有气体除外),以下说法正确的是( )
| A. | 原子半径和离子半径均减小 | |
| B. | 金属性减弱,非金属性增强 | |
| C. | 氧化物对应的水化物碱性减弱,酸性增强 | |
| D. | 单质的熔点降低 |
13.温度为T时,向2.0L恒容密闭容器中充入1.0mol PCl5,反应PCl5(g)?PCl3(g)+Cl2(g)经过一段时间后达到平衡.反应过程中测定的部分数据见表:
下列说法不正确的是( )
| t/s | 0 | 50 | 150 | 250 | 350 |
| n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
| A. | 反应在前50s的平均速率v(Cl2)=0.0016 mol•L-1•min-1 | |
| B. | 保持其他条件不变,升高温度,平衡时c(PCl3)=0.11 mol•L-1,则该反应的△H<0 | |
| C. | 温度为T时,起始时向容器中充入1.0 mol PCl5、0.20 mol PCl3和0.20 mol Cl2,反应达到平衡前v(正)>v(逆) | |
| D. | 温度为T时,起始时向容器中充入0.5 mol PCl3和0.5 mol Cl2,达到平衡时,PCl3的转化率小于80% |
10.下列反应,最终无沉淀产生的是( )
| A. | SO2通入盐酸酸化的硝酸钡溶液 | B. | 在AlCl3溶液中滴入过量的氨水 | ||
| C. | 在空气中长期存放的漂白粉溶液 | D. | 将少量NaAlO2投入盐酸中 |
17.下列有关化学用语表示正确的是( )
| A. | 四氯化碳分子的电子式为: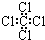 | |
| B. | C1-的结构示意图: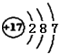 | |
| C. | 醋酸的电离方程式:CH3COOH+H2O?CH3COO-+H3O+ | |
| D. | 聚丙烯的结构简式: |
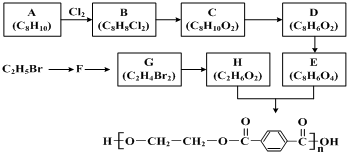
 ;
; (写出结构简式).
(写出结构简式). ,新戊烷的结构简式为C(CH3)4.
,新戊烷的结构简式为C(CH3)4.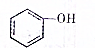 (填“>”、“<”或“=”,下同)
(填“>”、“<”或“=”,下同)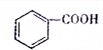 (提示:类比醇与酚的酸性)
(提示:类比醇与酚的酸性) .
. .
.