题目内容
5.对于${\;}_{1}^{1}$H和${\;}_{1}^{2}$H+两种粒子,下列叙述正确的是( )| A. | 质子数一定相同,质量数和中子数一定不同 | |
| B. | 化学性质几乎完全相同 | |
| C. | 一定都由质子、中子、电子构成 | |
| D. | 核电荷数,核外电子数一定相同 |
分析 原子符号ZAX中,元素符号左下角的数字为质子数,左上角的数字为质量数,右上角为离子所带电荷数,质子数=核电荷数=核外电子数,质子数+中子数=质量数.
解答 解:A、${\;}_{1}^{1}$H和${\;}_{1}^{2}$H+两种粒子的质子数为1,质量数分别为1、2,中子数分别为0,1,质子数一定相同,质量数和中子数一定不同,故A正确;
B、因质子数相同,则为同种元素的微粒,同种元素的原子和离子的化学性质不同,故B错误;
C、${\;}_{1}^{1}$H原子中,中子数为0,没有中子,故C错误;
D、${\;}_{1}^{1}$H的质子数等于核外电子数,${\;}_{1}^{2}$H+的质子数比核外电子数多,故D错误;
故选A.
点评 本题考查原子的表示方法及原子中的数量关系,明确质子数=核电荷数=核外电子数,质子数+中子数=质量数即可解答,题目较简单.

练习册系列答案
相关题目
5.为除去括号内的杂质,所选用的试剂或方法不正确的是( )
| A. | Na2CO3溶液(NaHCO3),选用适量的NaOH溶液 | |
| B. | NaHCO3溶液(Na2CO3),应通入过量的CO2气体 | |
| C. | Na2O2粉末(Na2O),将混合物在氧气中加热 | |
| D. | Na2CO3溶液(Na2SO4),加入适量Ba(OH)2溶液,过滤 |
6.下列说法正确的是( )
| A. | MgF2晶体中的化学键是共价键 | |
| B. | 某化合物在熔融态能导电,则该物质中一定含有离子键 | |
| C. | N2和HCl两种分子中,每个原子的最外层都具有8电子稳定结构 | |
| D. | 干冰是分子晶体,其溶于水生成碳酸的过程只需克服分子间作用力 |
3.某溶液中有Ca2+、NH${\;}_{4}^{+}$、Mg2+、Fe2+和Al3+五种离子,若向其中加入过量的氢氧化钠溶液微热并搅拌,再加入过量盐酸,溶液中的阳离子基本不减少的是( )
| A. | NH${\;}_{4}^{+}$ | B. | Mg2+ | C. | Fe2+ | D. | Al3+ |
10.下列涉及有机物的说法正确的是( )
| A. | 乙烯、氯乙烯、苯乙烯都是不饱和烃,均可用于合成有机高分子材料 | |
| B. | 苯能与溴发生取代反应,因此不能用苯萃取溴水中的溴 | |
| C. | 酒越陈越香是因为酒中含有的有机酸与乙醇生成了酯 | |
| D. | 糖类、蛋白质、脂肪都是重要的营养物质,它们都属于高分子化合物 |
10.关于${\;}_{16}^{34}$S的叙述正确的是( )
| A. | 核电荷数为34 | B. | 中子数为16 | C. | 核外电子数为18 | D. | 原子序数为16 |
17.将一定量的氯气通入30mL浓度为10.00mol/L的氢氧化钠浓溶液中,加热少许时间后溶液中形成NaCl、NaClO、NaClO3共存体系.下列判断不正确的是( )
| A. | 若反应中转移的电子为n mol,则n一定大于0.15 mol | |
| B. | n(NaCl):n(NaClO):n(NaClO3)可能为7:2:1 | |
| C. | 与NaOH反应的氯气一定为0.15 mol | |
| D. | n(Na+):n(Cl-) 可能为7:3 |
14.物质的结构决定物质的性质.请回答下列涉及物质结构和性质的问题: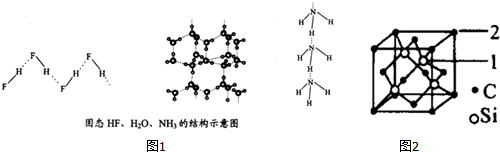
(1)第二周期中,元素的第一电离能处于B与N之间的元素有3种.
(2)某元素位于第四周期Ⅷ族,其基态原子的未成对电子数与基态碳原子的未成对电子数相同,则其基态原子的价层电子排布式为3d84s2
(3)乙烯酮(CH2═C═O)是一种重要的有机中间体,可用CH3COOH在(C2H5O)3P═O存在下加热脱H2O得到.乙烯酮分子中碳原子杂化轨道类型是sp2和sp,1mol(C2H5O)3P═O分子中含有的σ键的数目为25NA.
(4)已知固态NH3、H2O、HF的氢键键能和结构如表:
解释H2O、HF、NH3沸点依次降低的原因单个氢键的键能是(HF)n>冰>(NH3)n,而平均每个分子含氢键数:冰中2个,(HF)n和(NH3)n只有1个,气化要克服的氢键的总键能是冰>(HF)n>(NH3)n.
(5)碳化硅的结构与金刚石类似(如图2所示),其硬度仅次于金刚石,具有较强的耐磨性能.碳化硅
晶胞结构中每个碳原子周围与其距离最近的硅原子有4个,与碳原子等距离最近的碳原子有12个.已知碳化硅晶胞边长为apm,则碳化硅的密度为$\frac{1.6×1032}{NA•a3}$g•cm3.

(1)第二周期中,元素的第一电离能处于B与N之间的元素有3种.
(2)某元素位于第四周期Ⅷ族,其基态原子的未成对电子数与基态碳原子的未成对电子数相同,则其基态原子的价层电子排布式为3d84s2
(3)乙烯酮(CH2═C═O)是一种重要的有机中间体,可用CH3COOH在(C2H5O)3P═O存在下加热脱H2O得到.乙烯酮分子中碳原子杂化轨道类型是sp2和sp,1mol(C2H5O)3P═O分子中含有的σ键的数目为25NA.
(4)已知固态NH3、H2O、HF的氢键键能和结构如表:
| 物质 | 氢键X-H…Y | 键能KJ•mol-1 |
| (HF)n | F-H…F | 28.1 |
| 冰 | O-H…O | 18.8 |
| (NH3)n | N-H…N | 5.4 |
(5)碳化硅的结构与金刚石类似(如图2所示),其硬度仅次于金刚石,具有较强的耐磨性能.碳化硅
晶胞结构中每个碳原子周围与其距离最近的硅原子有4个,与碳原子等距离最近的碳原子有12个.已知碳化硅晶胞边长为apm,则碳化硅的密度为$\frac{1.6×1032}{NA•a3}$g•cm3.