题目内容
9.纯碱是一种非常重要的化工原料,纯碱属于( )| A. | 碱 | B. | 盐 | C. | 氧化物 | D. | 有机物 |
分析 电离出的阴离子全部是氢氧根离子的化合物是碱;
由金属阳离子和酸根阴离子组成的化合物为盐;
氧化物是指由两种元素组成且其中一种是氧元素的化合物.
有机物是含碳的化合物,有些含碳化合物性质与无机物相同一般也是无机物,如一氧化碳、二氧化碳、碳酸钙等.
解答 解:纯碱化学式是Na2CO3,是由钠离子和碳酸根离子构成的盐,含有三种元素,不属于氧化物,有机物是含碳的化合物,有些含碳化合物性质与无机物相同,一般归为无机物范畴,如一氧化碳、二氧化碳、碳酸钠等,所以碳酸钠不属于有机物,
故选B.
点评 本题主要考查学生对化学用语的书写及物质的分类,熟记常见物质的名称、化学式;掌握物质的简单分类是解答本题的关键,题目较简单.

练习册系列答案
相关题目
19.根据如图的转化关系判断下列说法正确的是(反应条件已略去)( )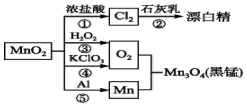

| A. | 反应①②③④⑤均属于氧化还原反应,反应③还属于置换反应 | |
| B. | 反应⑤说明该条件下铝可用于制熔点较高的金属 | |
| C. | 相同条件下生成等量的O2,反应③和④转移的电子数之比为1:1 | |
| D. | 反应①中氧化剂与还原剂的物质的量之比为1:4 |
17.下列图示与对应的叙述相符的是( )
| A. | 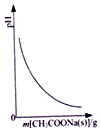 图表示向CH3COOH溶液中逐步加入CH3COONa固体后,溶液pH的变化 | |
| B. | 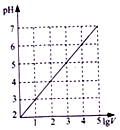 图表示0.1LpH=2的HC1溶液加水稀释至VL,pH随lgV的变化 | |
| C. | 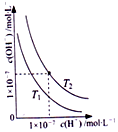 图表示不同温度下水溶液中H+和OH-浓度变化的曲线,图中温度T2>T1 | |
| D. | 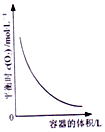 图表示同一温度下,再不同容积的容器中进行反应2BaO2(s)?2BaO(S)+O2(g),O2的平衡浓度与容器容积的关系 |
4.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 2.3g钠与水反应产生组气的分子数为0.05NA | |
| B. | 28gN2和N4组成的混合气体中含有的原子数为3NA | |
| C. | 0.1 mol•L-1Na2SO4溶液含有0.1NA个SO42- | |
| D. | 22.4L氯气中含有的电子总数一定为34NA |
14.下列物质中,属于共价化合物的是( )
| A. | NH4Cl | B. | H2SO4 | C. | CaCl2 | D. | K0H |
1.用NA表示阿伏加德罗常数的值.下列说法正确的是( )
| A. | 1 mol NO中含有的原子数目为2NA | |
| B. | 常温下,22.4L氮气含有的原子数目为2NA | |
| C. | 1L1 mol L-1 MgS04溶液中含有的Mg2+数目为2NA | |
| D. | 2.8 g硅单质与足量氧气在高温下完全反应时,硅原子失去的电子数目为2NA |
18.下列过程中反应离子方程式正确的是( )
| A. | 用漂白液漂洗衣物:H2O+2NaClO+CO2═2HClO+CO32-+2Na+ | |
| B. | 用碳酸钠溶液浸泡锅炉水垢:CaSO4(S)+CO32-(aq)?CaCO3(S)+SO42-(aq) | |
| C. | 用氢氧化钠溶液处理工业含二氧化硫的尾气:SO2+2OH-═HSO3-+H2O | |
| D. | 用加少量铁粉的方法存放硫酸亚铁溶液:Fe3++Fe═2Fe2+ |
19.下列有关实验的说法正确的是( )
| A. | 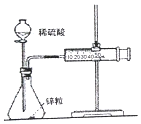 图中测定锌粒与1 mol•L-1 稀硫酸的反应速率,只需测定注射器中收集氢气的体积 | |
| B. | 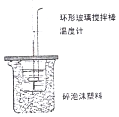 图 装置中进行50 mL 0.50 mol•L-1盐酸与50 mL 0.55 mol•L-1 NaOH 溶液发生中和反应放出热量的测定,使温度计温度升高的热量就是中和反应生成1 mol 水的热量 | |
| C. | 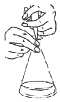 图 酸碱中和滴定中,可以在滴定过程中用少量水冲洗锥形瓶内壁 | |
| D. | 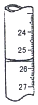 图滴定管中液面位置如图所示,则此时的读数为26.50 mL |
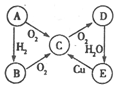 A、B、C、D、E五种物质中含有同一种元素,其相互转化关系如图所示.
A、B、C、D、E五种物质中含有同一种元素,其相互转化关系如图所示.