题目内容
19.下列有关实验的说法正确的是( )| A. | 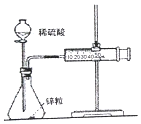 图中测定锌粒与1 mol•L-1 稀硫酸的反应速率,只需测定注射器中收集氢气的体积 | |
| B. | 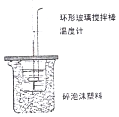 图 装置中进行50 mL 0.50 mol•L-1盐酸与50 mL 0.55 mol•L-1 NaOH 溶液发生中和反应放出热量的测定,使温度计温度升高的热量就是中和反应生成1 mol 水的热量 | |
| C. | 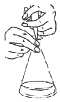 图 酸碱中和滴定中,可以在滴定过程中用少量水冲洗锥形瓶内壁 | |
| D. | 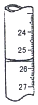 图滴定管中液面位置如图所示,则此时的读数为26.50 mL |
分析 A.需测定一定时间生成气体的体积;
B.50 mL 0.50 mol•L-1盐酸与50 mL 0.55 mol•L-1 NaOH 溶液发生中和反应不生成1 mol 水,且Q=cm△T;
C.用少量水冲洗锥形瓶内壁,不需要干燥或润洗;
D.刻度在25~26之间.
解答 解:A.需测定一定时间生成气体的体积,则不测定时间,不能测定反应速率,故A错误;
B.50 mL 0.50 mol•L-1盐酸与50 mL 0.55 mol•L-1 NaOH 溶液发生中和反应不生成1 mol 水,且Q=cm△T,则使温度计温度升高的热量不是中和反应生成1 mol 水的热量,故B错误;
C.用少量水冲洗锥形瓶内壁,不需要干燥或润洗,则图中操作合理,故C正确;
D.刻度在25~26之间,则此时的读数为25.50 mL,故D错误;
故选C.
点评 本题考查化学实验方案的评价,为高频考点,把握实验装置的作用、反应速率测定、中和热测定、中和滴定、实验技能为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
相关题目
9.纯碱是一种非常重要的化工原料,纯碱属于( )
| A. | 碱 | B. | 盐 | C. | 氧化物 | D. | 有机物 |
10.油条和豆浆是我国传统的早餐食物,炸油条时常用到一种白色物质,它既能中和发酵过程中产生的酸,又能起发泡作用,这种白色物质是( )
| A. | NaOH | B. | Ca(OH)2 | C. | NaHCO3 | D. | NaCl |
7.设NA表示阿伏加德罗常数的数值,则下列说法中正确的是( )
| A. | 常温常压下,8.0gCH4中含有的氢原子数为NA | |
| B. | 1mol氯气跟水完全反应,转移的电子数为2NA | |
| C. | 1 molNa2O2跟足量CO2完全反应,转移的电子数为NA | |
| D. | 0.1mol/L MgCl2溶液中含氯离子数为0.2NA |
4.若在加入铝粉能产生氢气的无色溶液中,分别加入下列各组离子,可能共存的是( )
| A. | NH4+、NO3-、Al3+、Cl- | B. | Na+、AlO2-、K+、NO3- | ||
| C. | MnO4-、K+、SO42-、Na+ | D. | AlO2-、K+、NO3-、OH- |
5.将足量的CO2不断通入NaOH、Ca(OH)2、NaAlO2的混合溶液中〔已知NaAlO2与CO2反应生成Al(OH)3〕,则生成沉淀的物质的量与通入CO2的体积的关系可表示为( )
| A. | 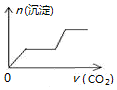 | B. | 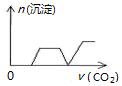 | C. | 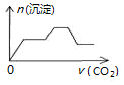 | D. |  |
3.下列说法正确的是( )
| A. | 石油的裂解、煤的干馏、蛋白质的盐析都是化学变化 | |
| B. | C2H4Cl2、C5H12均只有两种同分异构体 | |
| C. | Na与H2O的反应是熵增的放热反应,该反应能自发进行 | |
| D. | 已知25℃、101kPa,在稀溶液中:H+ (aq)+OH-(aq)=H2O(aq)△H=-57.3kJ/mol.则相同条件下,若将含1molCH3COOH的稀溶液与含1molNaOH的稀溶液混合,放出的热量等于57.3kJ |
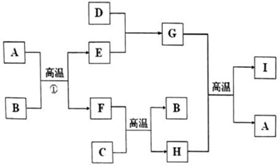 有关物质的转化关系如图所示(部分物质与条件己略去).A是最常见的无色液体,B、C是常见的金属单质,D、E是气体单质,且D在空气中的含量最多,F 是一种具有磁性的化合物,H是既能与强酸反应又能与强碱反应的氧化物:I具有耐高温、抗冲击、导热性好的优良性质,广泛应用于电子工业、陶瓷工业中.
有关物质的转化关系如图所示(部分物质与条件己略去).A是最常见的无色液体,B、C是常见的金属单质,D、E是气体单质,且D在空气中的含量最多,F 是一种具有磁性的化合物,H是既能与强酸反应又能与强碱反应的氧化物:I具有耐高温、抗冲击、导热性好的优良性质,广泛应用于电子工业、陶瓷工业中. .
.