题目内容
18.下列各离子方程式中,属于水解反应的是( )| A. | HCO3-+H2O?H3O++CO32- | B. | NH4++H2O?NH3•H2O+OH- | ||
| C. | PO43-+H2O?HPO42-+OH- | D. | H2O+H2O?H3O++OH- |
分析 水解反应中有水参加反应,为弱酸离子或弱碱离子与水电离的氢离子或氢氧根离子结合生成弱电解质的反应,以此来解答.
解答 解:A.HCO3-+H2O?H3O++CO32-,是碳酸氢根离子的电离,故A不选;
B.既不是电离也不是水解,方程式书写错了,故B不选;
C.磷酸根离子的水解反应方程式,故C选;
D.水的电离方程式,故D不选;
故选C.
点评 本题考查离子反应,侧重水解的离子反应的考查,明确水解的离子反应、电离的离子反应、化学反应中的离子反应即可解答,注重反应类型的分析,题目难度不大.

练习册系列答案
 轻松暑假总复习系列答案
轻松暑假总复习系列答案
相关题目
6.在298K、1.01×105 Pa下,将22gCO2通入750mL 1mol•L-1 NaOH 溶液中充分反应,测得反应放出x kJ的热量.已知在该条件下,1molCO2通入1L2mol•L-1 NaOH溶液中充分反应放出y kJ的热量,则CO2与NaOH溶液反应生成NaHCO3的热化学方程式正确的是( )
| A. | CO2(g)+NaOH(aq)═NaHCO3(aq)△H=-(2y-x) kJ•mol-1 | |
| B. | CO2(g)+NaOH(aq)═NaHCO3(aq)△H=-(2x-y) kJ•mol-1 | |
| C. | CO2(g)+NaOH(aq)═NaHCO3(aq)△H=-(4x-y) kJ•mol-1 | |
| D. | CO2(g)+2NaOH(l)═2NaHCO3(l)△H=-(8x-2y) kJ•mol-1 |
13.下列叙述错误的是( )
| A. | 13C和14C属于同一种元素,它们互为同位素 | |
| B. | LiH、LiD、LiT的摩尔质量之比为8:9:10 | |
| C. | 两原子如果核外电子排布相同,则一定属于同种元素 | |
| D. | 阴离子的核外电子排布一定与上一周期稀有气体元素原子的核外电子排布相同 |
7.下列离子方程式书写错误的是( )
| A. | 足量的CO2通入氨水中:CO2+NH3•H2O═NH4++HCO3- | |
| B. | 除去CO2中的HCl气体:CO32-+2H+═CO2+2H2O | |
| C. | 自然界中溶洞的形成:CaCO3+CO2+2H2O═Ca2++2HCO3- | |
| D. | 用烧碱溶液吸收氯气的反应:Cl2+2OH-═Cl-+ClO-+H2O |
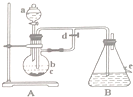 如图所示装置,可用来制取和观察Fe(OH)2在空气中被氧化的颜色变化.实验时必须使用铁屑和6mol/L的硫酸,其他试剂任选.填写下列空白:
如图所示装置,可用来制取和观察Fe(OH)2在空气中被氧化的颜色变化.实验时必须使用铁屑和6mol/L的硫酸,其他试剂任选.填写下列空白: