题目内容
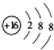
1.下列说法不正确的是(1)(2)(3)(5)(6)(7).(1)乙醛分子的比例模型:
 ; (2)铝离子的结构示意图:
; (2)铝离子的结构示意图: ;
;(3)次氯酸的结构式:H-OCl; (4)甲基的电子式:
(5)硫的原子结构示意图:
 ; (6)NH4Cl的电子式:
; (6)NH4Cl的电子式: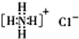 ;
;(7)原子核内有8个中子的氧原子${\;}_{8}^{18}$O.
分析 (1)比例模型能够体现出各原子的相对体积大小;
(2)铝离子的核电荷数为13;
(3)次氯酸的中心原子为O原子,应该用短线连接O和Cl原子;
(4)甲基为中性原子团,碳原子最外层为7个电子;
(5)硫的原子的核外电子总数为16,最外层含有6个电子;
(6)NH4Cl为离子化合物,电子式中氯离子需要标出最外层电子;
(7)原子核内有8个中子的氧原子的质量数为16,不是18.
解答 解:(1) 可表示乙醇的比例模型,乙醛的结构简式为CH3CHO,乙醛正确的比例模型为:
可表示乙醇的比例模型,乙醛的结构简式为CH3CHO,乙醛正确的比例模型为: ,故(1)错误;
,故(1)错误;
(2)铝离子的核电荷数为13,最外层含有8个电子,铝离子正确的结构示意图为: ,故(2)错误;
,故(2)错误;
(3)次氯酸分子中含有1个H-O键和1个O-H键,其正确的结构式为:H-O-Cl,故(3)错误;
(4)甲基中含有3个C-H键,为中性原子团,其电子式为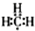 ,故(4)正确;
,故(4)正确;
(5) 为硫离子结构示意图,硫原子的核电荷数=核外电子总数=16,最外层含有6个电子,其正确的原子结构示意图为:
为硫离子结构示意图,硫原子的核电荷数=核外电子总数=16,最外层含有6个电子,其正确的原子结构示意图为: ,故(5)错误;
,故(5)错误;
(6)NH4Cl是离子化合物,由氨根离子与氯离子构成,电子式为 ,故(6)错误;
,故(6)错误;
(7)原子核内有8个中子的氧原子的质量数为16,其正确的表示方法为:816O,故(7)错误;
故答案为:(1)(2)(3)(5)(6)(7).
点评 本题考查了常见化学用语的表示方法,题目难度中等,涉及电子式、离子结构示意图、比例模型、结构简式等知识,明确常见化学用语的书写原则为解答关键,试题培养了学生的规范答题能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
16.从硫粉和铁粉的混合物中提取硫,最合理的方法是( )
| A. | 用磁铁分离出混合物中的铁粉 | B. | 将混合物溶于二硫化碳后过滤 | ||
| C. | 将混合物溶解于稀盐酸后过滤 | D. | 将混合物加热升华 |
3.原子序数依次增大的短周期主族元素a、b、c、d,它们的最外层电子数分别为1、4、1、4.a-的L层电子的电子数为0.下列说法正确的是( )
| A. | 元素b、c在同一周期 | |
| B. | 元素a、b、d各自最高和最低化合价的代数和均为0 | |
| C. | b的最高价氧化物对应的水化物酸性比d的弱 | |
| D. | 元素a、b、c不能存在于同一离子化合物中 |
6.下列关于金属元素特征的叙述中,正确的是( )
①金属元素的原子只有还原性,离子只有氧化性
②金属元素在化合物中都显正价
③元素的金属性越强,相应的离子氧化性越弱
④失电子数越多,元素的金属性越强.
①金属元素的原子只有还原性,离子只有氧化性
②金属元素在化合物中都显正价
③元素的金属性越强,相应的离子氧化性越弱
④失电子数越多,元素的金属性越强.
| A. | .①②③ | B. | ②③ | C. | ① | D. | 全部 |
10.将3.2g铜与过量浓硫酸共热反应,下列叙述中错误的是( )
| A. | 铜片溶解,生成物冷却后加水稀释溶液成蓝色 | |
| B. | 生成的气体体积为1.12L | |
| C. | 参加反应的硫酸与被还原的硫酸物质的量之比为2:1 | |
| D. | 该实验中可用NaOH溶液处理尾气 |
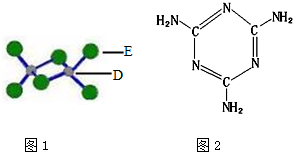 A、B、C、D、E为原子序数依次增大的短周期元素,B、C相邻且同周期,C原子中含有8种运动状态不同的电子.A、C能形成两种化合物甲和乙,原子个数比分别为2:1和1:1,甲为常见的溶剂.D是地壳中含量最多的金属元素.E元素为同周期电负性最大的元素.E和D可形成化合物丙.F为第四周期未成对电子数最多的元素
A、B、C、D、E为原子序数依次增大的短周期元素,B、C相邻且同周期,C原子中含有8种运动状态不同的电子.A、C能形成两种化合物甲和乙,原子个数比分别为2:1和1:1,甲为常见的溶剂.D是地壳中含量最多的金属元素.E元素为同周期电负性最大的元素.E和D可形成化合物丙.F为第四周期未成对电子数最多的元素