题目内容
4.在100℃时,将0.100mol的N2O4气体充入1L抽空密闭容器中,发生反应:N2O4(g)?2NO2.现在隔一定时间对该容器内的物质进行分析,得到如下表格:
| t/s c/(mol•L-1) | 0 | 20 | 40 | 60 | 80 | 100 |
| c(N2O4)/(mol•L-1) | 0.100 | c1 | 0.050 | c3 | a | b |
| c(NO2)/(mol•L-1) | 0 | 0.060 | c2 | 0.120 | 0.120 | 0.120 |
(1)达到平衡时N2O4的转化率为60%,表中c2>c3,a=b(后两空选填>、<、=)
(2)20s的N2O4的浓度c1=0.07mol/L在0~20s内N2O4的平均反应速率为0.0015mol/(L•s);
(3)若其他反应条件以及初始物质物质的量不变,将反应的温度降低到80℃时,达到平衡时NO2的物质的量为0.100mol,那么正反应是吸热反应(选填吸热或放热)
(4)若在相同初始情况下最初向该容器充入的是二氧化氮气体,要达到上述同样的平衡状态,二氧化氮的起始浓度为0.20mol/L.
分析 (1)由表可知,60s时反应达平衡,根据方程式计算△c(N2O4),根据转化率计算平衡时N2O4的转化率;
根据方程式计算,计算c2、c3,据此解答;
60s后反应达平衡,反应混合物各组分的浓度不变.
(2)由△c(NO2),根据方程式计算△c(N2O4),20s的四氧化二氮的浓度=起始浓度-△c(N2O4);
根据v=$\frac{△c}{△t}$计算v(N2O4).
(3)80℃时,达到平衡时NO2的物质的量为0.100mol,说明降低温度后平衡向着逆向移动,据此判断反应热;
(4)达到上述同样的平衡状态,说明两个平衡为等效平衡,按化学计量数换算到N2O4一边,满足c(N2O4)为0.100mol/L.
解答 解:(1)由表可知,60s时反应达平衡,c(NO2)=0.120mol/L,根据反应N2O4?2NO2可知,平衡时消耗二氧化氮的浓度为:c(N2O4)=0.120mol/L×$\frac{1}{2}$=0.06mol/L,则平衡时N2O4的转化率为:$\frac{0.06mol/L}{0.1mol/L}$×100%=60%;
达到平衡时各组分的浓度不再变化,则c3=a=b=0.1mol/L-0.06mol/L=0.04mol/L;
由表可知,40s时,c(N2O4)=0.050mol/L,N2O4的浓度变化为:(0.1-0.05)mol/L=0.05mol/L,则c2=0.05mol/L×2=0.10mol/L,所以c2>c3,
故答案为:60;>;=;
(2)由表可知,20s时,c(NO2)=0.060mol/L,则反应消耗 N2O4的浓度为0.030mol/L,则20s的四氧化二氮的浓度c1=0.1mol/L-0.03mol/L=0.07mol/L;
在0s~20s内四氧化二氮的平均反应速率为v(N2O4)=$\frac{0.03mol/L}{20s}$=0.0015mol•(L•s)-1,
故答案为:0.07mol/L;0.0015;
(3)若其他反应条件以及初始物质物质的量不变,将反应的温度降低到80℃时,达到平衡时NO2的物质的量为0.100mol<0.120mol/L,说明降低温度后平衡向着放热的逆向移动,则逆向为放热反应,故正反应为吸热反应,
故答案为:吸热;
(4)达到上述同样的平衡状态,为等效平衡,按化学计量数换算到N2O4一边,满足c(N2O4)为0.100mol/L即可,根据反应N2O4 ?2 NO2可知二氧化氮的浓度应该为:c(NO2)=2c(N2O4)=0.1mol/L×2=0.20mol/L,
故答案为:0.20mol/L.
点评 本题考查化学平衡的有关计算,题目难度中等,涉及化学反应速率、转化率等的计算、等效平衡的应用等知识,注意掌握化学反应速率、转化率的概念及表达式,明确等效平衡的判断方法为解答关键,试题培养了学生的分析能力及化学计算能力.

 水是生命的源泉,工业的血液、城市的命脉,要保护好河流,河水是重要的饮用水源,污染物通过用水直接毒害人体,也可通过食物链和灌溉农田间接危及健康.请问答下列问题:
水是生命的源泉,工业的血液、城市的命脉,要保护好河流,河水是重要的饮用水源,污染物通过用水直接毒害人体,也可通过食物链和灌溉农田间接危及健康.请问答下列问题:(1)25℃时,向水的电离平衡体系中加入少量碳酸钠固体,得到pH为11的溶液,其水解的离子方程式为CO32-+H2O?HCO3-+OH-、HCO3-+H2O?H2CO3+OH-,由水电离出c(OH-)=0.001mol•L-1.
(2)纯水在100℃时,pH=6,该温度下1mol.L-1的NaOH溶液中,由水电离出的c(OH-)=10-12mol•l-1
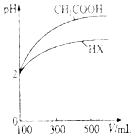
(3)体积均为100mL、pH均为2的CH3COOH溶液与一元酸HX溶液,加水稀释过程中pH与体积的关系如图所示,则HX的电离平衡常数小于(填“大于”“小于”或“等于”)CH3COOH的电离平衡常数.
(4)电离平衡常数是衡量弱电解质电离程度强弱的物理置.己知:
| 化学式 | 电离平衡常数(25℃) |
| HCN | K=4.9×10-10 |
| CH3COOH | K=1.8×10-5 |
| H2CO3 | K1=4.3x10-7,K2=5.6×10-11 |
②向NaCN溶液中通入少量的CO2,发生反应化学方程式为NaCN+H2O+CO2=HCN+NaHCO3.
(5)25℃时,在CH3COOH与CH3COONa的混合洛液中,若测得pH=6,则溶液中CH3COO-)•c(Na+)=9.9×10-7(填精确值)mol•L-1.
 铁及其化合物在日常生活、生产中应用广泛,研究铁及其化合物的应用意义重大.回答下列问题:
铁及其化合物在日常生活、生产中应用广泛,研究铁及其化合物的应用意义重大.回答下列问题:(1)已知高炉炼铁过程中会发生如下反应:
FeO(s)+CO(g)═Fe(s)+CO2(g)△H1
Fe2O3(s)+$\frac{1}{3}$CO(g)═$\frac{2}{3}$Fe3O4(s)+$\frac{1}{3}$CO2(g)△H2
Fe3O4(s)+CO(g)═3Fe(s)+CO2(g)H3
Fe2O3(s)+CO(g)═2Fe(s)+3CO2(g)H4
则△H4的表达式为△H2+$\frac{2}{3}$△H3(用含△H1、△H2、△H3的代数式表示).
(2)上述反应在高炉中大致分为三个阶段,各阶段主要成分与温度的关系如下:
| 温度 | 250℃ | 600℃ | 1000℃ | 2000℃ |
| 主要成分 | Fe2O3 | Fe3O4 | FeO | Fe |
(3)铁等金属可用作CO与氢气反应的催化剂.已知某种催化剂可用来催化反应 CO(g)+3H2(g)?CH4(g)+H2O(g)△H<0.在T℃,106Pa时将l mol CO和3mol H2加入体积可变的密闭容器中.实验测得CO的体积分数x(CO)如下表:
| t/min | 0 | 10 | 20 | 30 | 40 | 50 |
| x(CO) | 0.25 | 0.23 | 0.214 | 0.202 | 0.193 | 0.193 |
a.容器内压强不再发生变化 b.混合气体的密度不再发生变化
c.v正(CO)=3v逆(H2) d.混合气体的平均相对分子质量不再发生变化
②达到平衡时CO的转化率为37.1%;在T℃106Pa时该反应的压强平衡常数Kp(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)的计算式为$\frac{(\frac{0,371}{3.258})^{2}}{0.193×(\frac{1.887}{3.258})^{3}×1{0}^{12}P{a}^{2}}$;
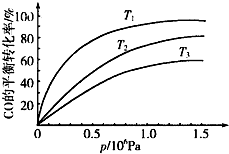
③图表示该反应CO的平衡转化率与温度、压强的关系.图中温度T1、T2、T3由高到低的顺序是T3>T2>T1,理由是正反应放热,在相同压强下,温度降低,平衡向正反应方向移动,CO的转化率越高.
| A. | 升高温度,平衡常数K变大 | |
| B. | 增大压强,W(g)物质的量分数变大 | |
| C. | 升温,若混合气体的平均相对分子质量变小,则正反应放热 | |
| D. | 增大X浓度,平衡向正反应方向移动 |
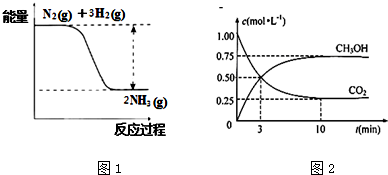
| A. | 新的平衡体系中,N2的浓度小于2c mol/L大于c mol/L | |
| B. | 新的平衡体系中,NH3的浓度小于2c mol/L大于c mol/L | |
| C. | 新的平衡体系中,混合气体的平均摩尔质量小于$\overline{M}$ | |
| D. | 新的平衡体系中,气体的密度是原平衡体系的1倍 |
已知:①2C3H8(g)+7O2(g)=6CO(g)+8H2O(l);△H=-2741.8kJ/mol
②2CO(g)+O2(g)=2CO2(g)△H=-566kJ/mol
(1)反应C3H8(g)+5O2(g)=3CO2(g)+4H2O(l)的△H=-2219.9KJ/mol
(2)C3H8在不足量的氧气里燃烧,生成CO和CO2以及气态水,将所有的产物通入一个固定体积的密闭容器中,在一定条件下发生如下可逆反应:CO (g)+H2O(g)?CO2(g)+H2 (g)
①下列事实能说明该反应达到平衡的是bd.
a.体系中的压强不发生变化 b.υ正(H2)=υ逆(CO)
c.混合气体的平均相对分子质量不发生变化 d.CO2的浓度不再发生变化
②T℃时,在一定体积的容器中,通入一定量的CO(g)和H2O(g),发生反应并保持温度不变,各物质浓度随时间变化如表:
| 时间/min | CO | H2O(g) | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | 0.100 | 0.200 | 0.100 | 0.100 |
| 4 | 0.100 | 0.200 | 0.100 | 0.100 |
| 5 | 0.116 | 0.216 | 0.084 | C1 |
| 6 | 0.096 | 0.266 | 0.104 | C2 |
已知420℃时,该化学反应的平衡常数为9.如果反应开始时,CO和H2O(g)的浓度都是0.01mol/L,则CO在此条件下的转化率为75%.又知397℃时该反应的平衡常数为12,请判断该反应的△H<0 (填“>”、“=”、“<”).
(3)依据(1)中的反应可以设计一种新型燃料电池,一极通入空气,另一极通入丙烷气体;燃料电池内部是熔融的掺杂着氧化钇(Y2O3)的氧化锆(ZrO2)晶体,在其内部可以传导O2-.在电池内部O2-移向负极(填“正”或“负”);电池的负极反应式为C3H8+10O2--20e-=3CO2+4H2O.
(4)用上述燃料电池用惰性电极电解足量Mg(NO3)2和NaCl的混合溶液.电解开始后阴极的现象为有无色气体生成,有白色沉淀生成.
 (1)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有湿润有色布条的广口瓶,可观察到的现象是干燥的有色布条无明显现象,潮湿的有色布条褪色.
(1)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有湿润有色布条的广口瓶,可观察到的现象是干燥的有色布条无明显现象,潮湿的有色布条褪色.