题目内容
在如图点滴板上有四个溶液间反应的小实验,其对应反应的离子方程式书写正确的是( )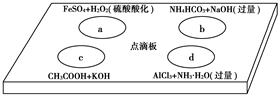

| A、a反应:Fe2++2H++H2O2═Fe3++2H2O |
| B、b反应:HCO3-+OH-═CO32-+H2O |
| C、c反应:H++OH-═H2O |
| D、d反应:Al3++3NH3?H2O═Al(OH)3↓+3NH4+ |
考点:离子方程式的书写
专题:
分析:A.电子、电荷不守恒;
B.漏写铵根离子与碱的反应;
C.醋酸在离子反应中保留化学式;
D.一水合氨在离子反应中保留化学式,生成氢氧化铝和氯化铵.
B.漏写铵根离子与碱的反应;
C.醋酸在离子反应中保留化学式;
D.一水合氨在离子反应中保留化学式,生成氢氧化铝和氯化铵.
解答:
解:A.离子方程式必须满足电荷守恒,正确的离子方程式为:2Fe2++2H++H2O2=2Fe3++2H2O,故A错误;
B.氢氧化钠过量,则铵根离子也参与反应,正确的离子方程式为:NH4++HCO3-+2OH-=CO32-+H2O+NH3?H2O,故B错误;
C.醋酸在离子反应中保留化学式,离子反应为CH3COOH+OH-=CH3COO-+H2O,故C错误;
D.反应生成氢氧化铝和氯化铵,离子反应为Al3++3NH3?H2O═Al(OH)3↓+3NH4+,故D正确;
故选D.
B.氢氧化钠过量,则铵根离子也参与反应,正确的离子方程式为:NH4++HCO3-+2OH-=CO32-+H2O+NH3?H2O,故B错误;
C.醋酸在离子反应中保留化学式,离子反应为CH3COOH+OH-=CH3COO-+H2O,故C错误;
D.反应生成氢氧化铝和氯化铵,离子反应为Al3++3NH3?H2O═Al(OH)3↓+3NH4+,故D正确;
故选D.
点评:本题考查离子反应书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)、检查是否符合原化学方程式等,题目难度不大.

练习册系列答案
相关题目
下列说法中正确的是( )
| A、在酸性环境中钢铁发生析氢腐蚀 |
| B、电解质溶液为氢氧化钠溶液,铝和镁形成原电池时,镁作负极 |
| C、铅蓄电池中铅做正极,PbO2做负极,两极浸在H2SO4溶液中 |
| D、镀层破损后,白铁(镀锌的铁)比马口铁(镀锡的铁)更易被腐蚀 |
已知Br2+2Fe2+═2Br-+2Fe3+,向FeBr2溶液中通入Cl2发生反应后,溶液中有一半的Br-被氧化,则FeBr2与Cl2物质的量之比是( )
| A、1:1 | B、2:3 |
| C、1:2 | D、3:5 |
某强酸性溶液中可能存在NO-3、Cl-、I-和Fe3+中的一种或几种.向该溶液中加入溴水,单质溴被还原,由此推断该溶液中( )
| A、不含NO-3,可能含Fe3+ |
| B、含有NO3-、Cl-、I- |
| C、含I-,但不能确定是否含Cl- |
| D、含有Fe3+ |
宇宙飞船是用N2H4联氨与N2O4作为推力能源,其未配平的反应式为N2H4+N2O4→N2+H2O下列说法正确的是
( )
( )
| A、N2既是氧化产物又是还原产物 |
| B、氧化产物与还原产物物质的量之比为1:2 |
| C、联氨是氧化剂 |
| D、氧化剂与还原剂物质的量之比为2:1 |
下列离子方程式正确的是( )
| A、向盐酸中滴加氨水:H++OH-=H2O | ||||
B、氯化铵与氢氧化钠两种浓溶液混合加热:NH4++OH-
| ||||
| C、氢氧化镁与稀硫酸反应:H++OH-═H2O | ||||
| D、单质铜与稀硝酸反应:Cu+2H++2NO3-═Cu2++2NO↑+H2O |
 某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的氢氧化钠溶液时,选择甲基橙作指示剂.请填写下列空白:
某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的氢氧化钠溶液时,选择甲基橙作指示剂.请填写下列空白: )过去常被用来做面粉增白剂,但目前已被禁用.合成过氧化苯甲酰的流程如下:
)过去常被用来做面粉增白剂,但目前已被禁用.合成过氧化苯甲酰的流程如下:
 )能与水反应生成苯甲酸,同样也能与乙醇反应,写出其与乙醇反应生成有机产物的名称
)能与水反应生成苯甲酸,同样也能与乙醇反应,写出其与乙醇反应生成有机产物的名称