题目内容
某强酸性溶液中可能存在NO-3、Cl-、I-和Fe3+中的一种或几种.向该溶液中加入溴水,单质溴被还原,由此推断该溶液中( )
| A、不含NO-3,可能含Fe3+ |
| B、含有NO3-、Cl-、I- |
| C、含I-,但不能确定是否含Cl- |
| D、含有Fe3+ |
考点:氧化还原反应
专题:
分析:加入溴水,单质溴被还原,则溶液中一定含还原性离子,结合离子共存来解答.
解答:
解:加入溴水,单质溴被还原,则溶液中一定I-,而I-和Fe3+发生氧化还原反应不能共存,酸性溶液中NO-3、I-发生氧化还原反应不能共存,
则一定含I-,但不能确定是否含Cl-,一定不含NO3-、Fe3+,
故选C.
则一定含I-,但不能确定是否含Cl-,一定不含NO3-、Fe3+,
故选C.
点评:本题考查氧化还原反应和离子共存,为高频考点,把握离子之间的氧化还原反应为解答的关键,注重基础知识的考查,题目难度不大.

练习册系列答案
相关题目
下表是3种物质的溶解度(20℃),下列说法中正确的是( )
| 物质 | MgCl2 | Mg(OH)2 | MgCO3 |
| 溶解度(g/100g) | 74 | 0.000 84 | 0.01 |
| A、已知MgCO3的Ksp=6.82×10-6 mol2?L-2,则所有含有固体MgCO3的溶液中,都有c(Mg2+)=c(CO32-),且c(Mg2+)?c(CO32-)=6.82×10-6 mol2?L-2 |
| B、除去粗盐中含有的MgCl2杂质,最佳除杂试剂为Na2CO3溶液 |
| C、将表中三种物质与水混合,加热、灼烧,最终的固体产物相同 |
| D、用石灰水处理含有Mg2+和HCO3-的硬水,发生的离子反应方程式为Mg2++2HCO3-+Ca2++2OH-═CaCO3↓+MgCO3↓+2H2O |
工业上可利用甲烷除去NO气体,反应为CH4(g)+4NO(g)?CO2(g)+2N2(g)+2H2O(g)△H<0.在恒容的密闭容器中,下列有关说法正确的是( )
| A、平衡时,其他条件不变,升高温度可使该反应的平衡常数增大 |
| B、平衡时,其他条件不变,增加CH4的浓度,氮氧化物的转化率减小 |
| C、其他条件不变,使用高效催化剂,废气中氮氧化物的转化率增大 |
| D、单位时间内消耗CH4和N2的物质的量比为1:2时,反应达到平衡 |
我们生活在千变万化的物质世界里.下列过程或变化中,没有发生氧化还原反应的是( )
| A、iPhone5手机电池充电 |
| B、铁制品镀铜 |
| C、爆竹爆炸 |
| D、利用焰色反应检验Na+ |
在如图点滴板上有四个溶液间反应的小实验,其对应反应的离子方程式书写正确的是( )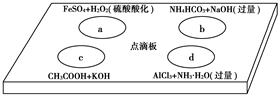

| A、a反应:Fe2++2H++H2O2═Fe3++2H2O |
| B、b反应:HCO3-+OH-═CO32-+H2O |
| C、c反应:H++OH-═H2O |
| D、d反应:Al3++3NH3?H2O═Al(OH)3↓+3NH4+ |
向1L 0.5mol/L的H2SO4溶液中加入10.1g KNO3和12.8g Cu,充分反应后产生的气体在标准状况下的体积为( )
| A、2.24L |
| B、3.36L |
| C、4.48L |
| D、5.60L |
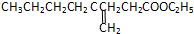
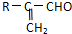
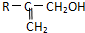
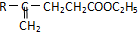
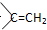 ,核磁共振氢谱有3个峰,且峰面积之比为9:2:1的同分异构体的结构简式为
,核磁共振氢谱有3个峰,且峰面积之比为9:2:1的同分异构体的结构简式为