题目内容
2.下列说法正确的是( )| A. | 20Ne和22Ne互为同位素 | |
| B. | 液氯和氯水是同一种物质 | |
| C. | 金刚石、石墨和富勒烯互为同分异构体 | |
| D. | 碘单质和碘蒸气互为同素异形体 |
分析 A.质子数相同中子数不同的同种元素的不同原子互称为同位素;
B.液氯是液态氯气,氯水为氯气的水溶液;
C.分子式相同结构不同的化合物为同分异构体,一般指有机化合物;
D.同素异形体是同种元素组成的不同单质.
解答 解:A.20Ne和22Ne质子数相同中子数不同的同种元素的不同原子互称为同位素,故A正确;
B.液氯是液态氯气是纯净物,氯水为氯气的水溶液属于混合物,故B错误;
C.分子式相同结构不同的化合物为同分异构体,金刚石、石墨和富勒烯是碳元素组成的不同单质,互为同素异形体,故C错误;
D.碘单质和碘蒸气是一种物质,故D错误;
故选A.
点评 本题考查了同位素、同素异形体、同分异构体概念的理解应用,掌握基础是解题关键,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
12.NA为阿伏伽德罗常数的值.下列叙述正确的是( )
| A. | 标准状况下,6.72L NO2与水充分反应转移的电子数目为0.2NA | |
| B. | 1mo1的Fe在1mo1Cl2中充分燃烧,转移电子数为3NA | |
| C. | 7.2g CaO2中的阴离子含有的电子数为1.0NA | |
| D. | 标准状况下,22.4L盐酸含有2NA个离子 |
13.将铁粉加入到一定量AgNO3、Cu(NO3)2的混合溶液中,充分反应后过滤,向滤渣中加入稀盐酸发现有气体逸出,则滤渣的组成为( )
| A. | 铁 | B. | 铁和铜 | C. | 铁和银 | D. | 铁、铜、银 |
7.下列关于化学用语叙述正确的是( )
| A. | H2O2的电子: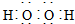 | |
| B. | 乙烯的结构简式:CH2CH2 | |
| C. | S2-离子的结构示意图: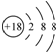 | |
| D. | FeSO4的电离方程式:FeSO4═Fe3++SO42- |
14.某水溶液中可能含有Na+、Al3+、Fe3+、Mg2+、Ba2+、NH4+、Cl-、SO42-离子中的若干种.某同学取200mL该溶液分成两等份依次进行如下实验:①向第一份溶液中加过量的NaOH溶液后加热,充分反应后生成0.02mol气体,无沉淀产生,同时得到溶液甲.②向溶液甲中通入过量的CO2气,充分反应生成白色沉淀,沉淀经过滤、洗涤、灼烧至恒重得到1.02g固体.③向第二份溶液中加入足量的BaCl2溶液,充分反应生成白色沉淀,沉淀用盐酸充分洗涤、干燥,得到11.65g固体.据此,该同学得到的结论正确的是( )
| A. | 实验①中产生的气体为氨,并可得原溶液中c(NH4+)=0.1 mol•L-1 | |
| B. | 实验③中的沉淀里一定有BaSO4,可能有Mg(OH)2 | |
| C. | 若要确定原溶液中是否含有Cl-,无需另外再设计实验验证 | |
| D. | 原溶液中一定含有Na+,且c(Na+)≥0.2 mol•L-1 |
11.下列操作或装置能达到实验目的是( )
| A. | 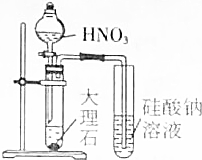 证明HNO3酸性比H2CO3强 | B. | 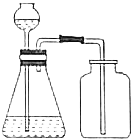 实验室用二氧化锰和盐酸制氯气 | ||
| C. | 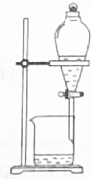 分离溴苯和苯 | D. | 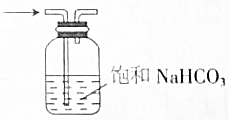 除去CO2中SO2 |
1.食醋的主要成分是乙酸,下列物质中,能与乙酸发生反应的是( )
①石蕊 ②乙醇 ③氢氧化铜 ④金属铝 ⑤氧化镁 ⑥碳酸钙.
①石蕊 ②乙醇 ③氢氧化铜 ④金属铝 ⑤氧化镁 ⑥碳酸钙.
| A. | ①③④⑤⑥ | B. | ②③④⑤ | C. | ①②④⑤⑥ | D. | 全部 |
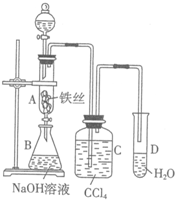 某化学课外小组用图装置制取溴苯.
某化学课外小组用图装置制取溴苯. .
.