题目内容
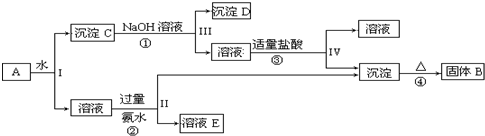
14.某水溶液中可能含有Na+、Al3+、Fe3+、Mg2+、Ba2+、NH4+、Cl-、SO42-离子中的若干种.某同学取200mL该溶液分成两等份依次进行如下实验:①向第一份溶液中加过量的NaOH溶液后加热,充分反应后生成0.02mol气体,无沉淀产生,同时得到溶液甲.②向溶液甲中通入过量的CO2气,充分反应生成白色沉淀,沉淀经过滤、洗涤、灼烧至恒重得到1.02g固体.③向第二份溶液中加入足量的BaCl2溶液,充分反应生成白色沉淀,沉淀用盐酸充分洗涤、干燥,得到11.65g固体.据此,该同学得到的结论正确的是( )| A. | 实验①中产生的气体为氨,并可得原溶液中c(NH4+)=0.1 mol•L-1 | |
| B. | 实验③中的沉淀里一定有BaSO4,可能有Mg(OH)2 | |
| C. | 若要确定原溶液中是否含有Cl-,无需另外再设计实验验证 | |
| D. | 原溶液中一定含有Na+,且c(Na+)≥0.2 mol•L-1 |
分析 ①第一份加过量NaOH溶液后加热,收集到0.02mol气体,即为氨气,一定含有NH4+,物质的量为0.02mol,浓度为:$\frac{0.02mol}{0.1L}$=0.2mol/L,无沉淀生成,则一定不含有Fe3+、Mg2+;
②向甲溶液中通入过量CO2,生成白色沉淀,即为氢氧化铝,则原溶液中一定有Al3+,一定不含有碳酸根离子,铝离子和过量的氢氧化钠反应生成偏铝酸钠溶液,溶液中通入过量CO2,生成白色沉淀,即为氢氧化铝,氢氧化铝沉淀经过滤、洗涤、灼烧后,得到1.02g固体即为氧化铝,根据铝元素守恒,得到铝离子的物质的量是$\frac{1.02g}{102g/mol}$×2=0.02mol,浓度为:$\frac{0.02mol}{0.1L}$=0.2mol/L;
③第二份加足量BaCl2溶液后,生成白色沉淀,则一定含有硫酸根离子,无钡离子.沉淀经足量盐酸洗涤、干燥后,得到11.65g固体即硫酸钡的质量是11.65g,物质的量为:$\frac{11.65g}{233g/mol}$=0.05mol,根据元素守恒,所以硫酸根离子的物质的量是0.05mol,浓度为:$\frac{0.05mol}{0.1L}$=0.5mol/L,
综上可知,一定含有的离子是:NH4+、Al3+、SO42-,其浓度分别是:0.2mol/L;0.2mol/L;0.5mol/L,一定不含Fe3+、Mg2+、Ba2+、SO42,不能确定是否存在氯离子.以此解答该题.
解答 解:①第一份加过量NaOH溶液后加热,收集到0.02mol气体,即为氨气,一定含有NH4+,物质的量为0.02mol,浓度为:$\frac{0.02mol}{0.1L}$=0.2mol/L,无沉淀生成,则一定不含有Fe3+、Mg2+;
②向甲溶液中通入过量CO2,生成白色沉淀,即为氢氧化铝,则原溶液中一定有Al3+,一定不含有碳酸根离子,铝离子和过量的氢氧化钠反应生成偏铝酸钠溶液,溶液中通入过量CO2,生成白色沉淀,即为氢氧化铝,氢氧化铝沉淀经过滤、洗涤、灼烧后,得到1.02g固体即为氧化铝,根据铝元素守恒,得到铝离子的物质的量是$\frac{1.02g}{102g/mol}$×2=0.02mol,浓度为:$\frac{0.02mol}{0.1L}$=0.2mol/L;
③第二份加足量BaCl2溶液后,生成白色沉淀,则一定含有硫酸根离子,无钡离子.沉淀经足量盐酸洗涤、干燥后,得到11.65g固体即硫酸钡的质量是11.65g,物质的量为:$\frac{11.65g}{233g/mol}$=0.05mol,根据元素守恒,所以硫酸根离子的物质的量是0.05mol,浓度为:$\frac{0.05mol}{0.1L}$=0.5mol/L,
综上可知,一定含有的离子是:NH4+、Al3+、SO42-,其浓度分别是:0.2mol/L;0.2mol/L;0.5mol/L,一定不含Fe3+、Mg2+、Ba2+、SO42,不能确定是否存在氯离子.
A.根据以上分析可知,c (NH4+)=0.2 mol•L-1,故A错误;
B.根据以上分析可知,③中的白色沉淀中一定有BaSO4,因溶液不存在镁离子,则没有生成氢氧化镁,故B错误;
C.由以上分析可知,不能确定存在氯离子,故C错误;
D.任何溶液中都存在电荷守恒,NH4+、Al3+、SO42-,其浓度分别是:0.2mol/L;0.2mol/L;0.5mol/L,可以知道NH4+、Al3+的正电荷总量小于SO42-负电荷总量,依据电荷守恒,则一定有Na+存在,若无氯离子存在,则0.2×1+0.2×3+c(Na+)×1=0.5×2,解得c(Na+)=0.2mol/L,若含有氯离子,c(Na+)>0.2mol/L,故D正确.
故选D.
点评 本题考查离子的检验,为高频考点,侧重于学生的分析、计算能力的考查,题目采用定性实验和定量计算分析相结合的模式,增大了解题难度,同时涉及离子共存、离子反应等都是解题需注意的信息,尤其是K+的确定易出现失误,题目难度中等.

 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案| A. | 过氧化钠放置在空气中,最终转变为白色粉末Na2CO3 | |
| B. | Ca(ClO)2溶液通入CO2,溶液变浑浊;再加入品红溶液,红色褪去 | |
| C. | 打磨过的铝箔和未打磨的铝箔分别在空气中灼烧,两种铝箔均熔化但不滴落,说明氧化铝熔点比铝高 | |
| D. | 在一定条件下,金属Na、Mg、Fe与水反应都生成H2和对应的碱 |
| A. | 20Ne和22Ne互为同位素 | |
| B. | 液氯和氯水是同一种物质 | |
| C. | 金刚石、石墨和富勒烯互为同分异构体 | |
| D. | 碘单质和碘蒸气互为同素异形体 |
| A. | 标准状况下,4.48 L乙醇中含有的分子数目为0.2NA | |
| B. | 常温常压下,6.4 g SO2中含有的氧原子数目为0.2NA | |
| C. | 1 L 0.1 mol•L-1 K2CO3溶液中含有的钾离子数目为0.1 NA | |
| D. | 100 mL 1.0 mol•L-1 FeCl3溶液与足量铜反应,转移的电子数目为0.2NA |
| A. | 煤 | B. | 天然气 | C. | 汽油 | D. | 氢气 |

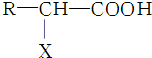 ,X的名称为氨基.
,X的名称为氨基. )易水解,其水解反应的产物为乙酸和
)易水解,其水解反应的产物为乙酸和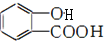 (填结构简式).
(填结构简式).