题目内容
7.有A、B、C、D、E五种短周期元素,元素A的一种原子无中子,元素B和C都有2个电子层,它们能生成无色无嗅的气体BC2,元素D有三个电子层,它和元素C属于同一主族,D和C生成有刺激性气味的气体DC2;元素E的阳离子E+的电子层结构与Ne的电子层结构相同,试回答:(1)它们的元素名称是:A氢B碳C氧D硫E钠.
(2)A与B的化合物以共价键结合,写出BA4的电子式
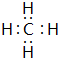 ;
;C和E的化合物以离子(或离子、共价)键结合,写出E2C的电子式
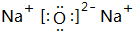 ;
;(3)A、B、C、E的原子半径从大到小的顺序为(写元素符号)Na>S>C>O>H;
(4)写出A和C的化合物(A2C)与C和E的化合物(E2C2)反应的化学方程式:2Na2O2+2H2O=4NaOH+O2↑.
分析 A、B、C、D、E五种元素,元素A的一种原子无中子,则A为氢元素;元素B和C都有2个电子层,它们能生成无色无嗅的气体BC2,则B为碳元素、C为O元素;元素D有三个电子层,它和元素C属于同一主族,则D为硫元素,硫和氧可以生成有刺激性气味的气体SO2;元素E的阳离子E+的电子层结构与Ne的电子层结构相同,则E为Na元素.
解答 解:A、B、C、D、E五种元素,元素A的一种原子无中子,则A为氢元素;元素B和C都有2个电子层,它们能生成无色无嗅的气体BC2,则B为碳元素、C为O元素;元素D有三个电子层,它和元素C属于同一主族,则D为硫元素,硫和氧可以生成有刺激性气味的气体SO2;元素E的阳离子E+的电子层结构与Ne的电子层结构相同,则E为Na元素.
(1)由上述分析可知,A为氢,B为碳,C为氧,D为硫,E为钠,
故答案为:氢;碳;氧;硫;钠;
(2)H与C可以形成CH4、HC≡CH等,以共价键相结合,CH4的电子式为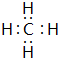 ,
,
O和Na可以形成氧化钠,也可以形成过氧化钠等,所以它们形成的化合物以离子键或离子键、共价键结合,Na2O的电子式为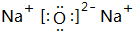 ,
,
故答案为:共价;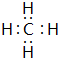 ;离子(或离子键、共价键);
;离子(或离子键、共价键);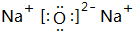 ;
;
(3)同周期自左而右原子半径减小,一般电子层越多原子半径越大,故原子半径Na>S>C>O>H,
故答案为:Na>S>C>O>H;
(4)A和C的化合物为H2O,C和E的化合物为Na2O2,二者反应的化学方程式:2Na2O2+2H2O=4NaOH+O2↑,
故答案为:2Na2O2+2H2O=4NaOH+O2↑.
点评 本题考查结构性质位置关系应用,关键是推断元素,侧重对化学式用语与元素周期律、元素化合物组成与性质的考查,难度不大,有利于基础知识的巩固.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
17.同周期的 IIA 族元素与IIIA族元素核电荷数相差不可能是( )
| A. | 1 | B. | 11 | C. | 17 | D. | 25 |
18.下列说法不正确的是( )
| A. | 催化剂是改变化学反应速率最有效的手段之一,使用催化剂可以带来巨大的经济效益 | |
| B. | 能量是可以互相转化的.植物的光合作用可将太阳能转变成化学能,太阳能电池可将光能转变成电能.原电池和电解池可实现化学能和电能的相互转换 | |
| C. | 有机高分子合成为人类提供了大量的新材料,聚氯乙烯、有机玻璃、腈纶、酚醛树脂等都属于合成高分子材料,都是通过加聚反应得到的 | |
| D. | 计算机技术的发展,使化学研究进入了分子水平,分子设计的思想为合成人类需要的新物质开辟了更广阔的道路 |
15.已知反应A2+B2═2AB,破坏1mol A2中的化学键消耗的能量为Q1 kJ,破坏1mol B2中的化学键消耗的能量为Q2 kJ,形成1mol AB中的化学键释放的能量为Q3 kJ,则下列说法正确的是( )
| A. | 若A2和B2的总能量大于生成的AB的总能量,则反应放热 | |
| B. | 若A2和B2的总能量小于生成的AB的总能量,则反应放热 | |
| C. | 若该反应为放热反应,则Q1+Q2>Q3 | |
| D. | 若该反应为吸热反应,则Q1+Q2>Q3 |
19.氧化还原反应在生产、生活中应用广泛.下列反应不属于氧化还原反应的是( )
| A. | 木炭燃烧:C+O2 $\frac{\underline{\;点燃\;}}{\;}$CO2 | |
| B. | 煅烧石灰石:CaCO3$\frac{\underline{\;点燃\;}}{\;}$ CaO+CO2↑ | |
| C. | 铁的冶炼:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 | |
| D. | 电解水:2H2O$\frac{\underline{\;通电\;}}{\;}$2 H2↑+O2↑ |
16.下列各组排列的顺序不正确的是( )
| A. | 离子半径:Na+>Mg2+>Al3+>F- | |
| B. | 热稳定性:HCl>H2S>PH3>AsH3 | |
| C. | 酸性强弱:Al(OH)3<H2SiO3<H2CO3<H2SO4 | |
| D. | 碱性强弱:KOH>NaOH>Mg(OH)2>Al(OH)3 |
 ;反应类型加聚反应.
;反应类型加聚反应.