题目内容
某研究性学习小组设计了一组实验来探究元素周期律.甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图1装置来一次性完成碳族元素中C与Si的非金属性强弱比较的实验研究;乙同学设计了如图2装置来验证卤族元素性质的递变规律.A、B、C三处分别是沾有NaBr溶液的棉花、湿润的淀粉KI试纸、湿润红纸.已知常温下浓盐酸与高锰酸钾能反应生成氯气.
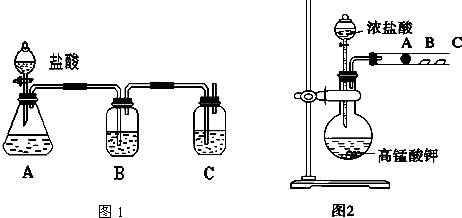
(1)甲同学设计实验的依据是 ;写出选用物质的化学式:A ,B ,C ;
其中装置B中所盛试剂的作用为 ;C中反应的离子方程式为 ;
(2)乙同学的实验原理是 ;写出B处的离子方程式: .

(1)甲同学设计实验的依据是
其中装置B中所盛试剂的作用为
(2)乙同学的实验原理是
考点:性质实验方案的设计
专题:实验题
分析:(1)根据信息知道:甲同学根据元素非金属性与对应最高价含氧酸之间的关系如图1装置来一次性完成C、Si三种非金属元素的非金属性强弱比较,根据强酸制弱酸来回答即可;B的作用是除去二氧化碳中氯化氢,C中二氧化碳和硅酸钠反应;
(2)根据氧化性强的单质可以将氧化性弱的单质从其盐中置换出来结合反应产物来分析.
(2)根据氧化性强的单质可以将氧化性弱的单质从其盐中置换出来结合反应产物来分析.
解答:
解:(1)根据题干信息:甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图1装置来一次性完成同主族元素非金属性强弱比较的实验研究,碳酸酸性强于硅酸,最高价氧化物对应水化物酸性越强,则原子的非金属性越强,依据强酸制弱酸来设计反应;A装置用来制取二氧化碳,故A为碳酸钙,盐酸易挥发,故B的作用是除去二氧化碳中氯化氢,故B为饱和碳酸钠溶液,C为硅酸钠溶液,二氧化碳和硅酸钠发生反应离子方程式为:SiO32-+CO2+H2O═H2SiO3↓+CO32-;
故答案为:强酸制弱酸;碳酸钙;饱和碳酸钠溶液;硅酸钠溶液;除去二氧化碳中氯化氢气体;SiO32-+CO2+H2O═H2SiO3↓+CO32-;
(2)根据题干信息:乙同学设计了如图2装置来验证卤族元素性质的递变规律,所以乙同学的实验原理是活泼的非金属单质置换较不活泼的非金属单质,高锰酸钾和浓盐酸反应会产生氯气,氯气具有氧化性,能将溴离子,碘离子氧化为对应的单质,即A处:Cl2+2Br-=2Cl-+Br2,B:Cl2+2I-=2Cl-+I2,
故答案为:活泼的非金属单质置换较不活泼的非金属单质;Cl2+2I-=2Cl-+I2.
故答案为:强酸制弱酸;碳酸钙;饱和碳酸钠溶液;硅酸钠溶液;除去二氧化碳中氯化氢气体;SiO32-+CO2+H2O═H2SiO3↓+CO32-;
(2)根据题干信息:乙同学设计了如图2装置来验证卤族元素性质的递变规律,所以乙同学的实验原理是活泼的非金属单质置换较不活泼的非金属单质,高锰酸钾和浓盐酸反应会产生氯气,氯气具有氧化性,能将溴离子,碘离子氧化为对应的单质,即A处:Cl2+2Br-=2Cl-+Br2,B:Cl2+2I-=2Cl-+I2,
故答案为:活泼的非金属单质置换较不活泼的非金属单质;Cl2+2I-=2Cl-+I2.
点评:本题将元素及其化合物、元素周期律与非金属性强弱比较的实验设计结合起来,具有较强的综合性,有一定的难度,注意实验设计的原理和方法

练习册系列答案
相关题目
水是生命之源.下列关于水的说法正确的是( )
| A、水属于非电解质 |
| B、氢氧两种元素只能组成水 |
| C、0℃时冰的密度比液态水的密度大 |
| D、标准状况下,18g水分子的物质的量为1mol |

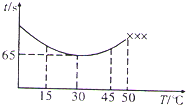 NaHSO4可被过量KIO3氧化,当NaHSO3.完全消耗时即有I2析出.某课题组用淀粉作指示剂,通过测定溶液变蓝所用时间来探究影响化学反应速率的因素.
NaHSO4可被过量KIO3氧化,当NaHSO3.完全消耗时即有I2析出.某课题组用淀粉作指示剂,通过测定溶液变蓝所用时间来探究影响化学反应速率的因素.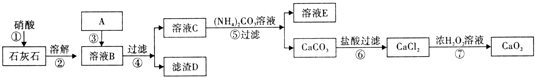
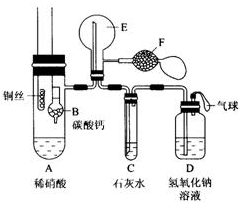 为了证明铜与稀硝酸反应产生一氧化氮,某校学生实验小组设计了一个实验,其装置如图所示(加热装置和固定装置均已略去).B为一个用金属丝固定的干燥管,内装块状碳酸钙固体;E为 一个空的蒸馏烧瓶;F是用于鼓入空气的双连打气球.
为了证明铜与稀硝酸反应产生一氧化氮,某校学生实验小组设计了一个实验,其装置如图所示(加热装置和固定装置均已略去).B为一个用金属丝固定的干燥管,内装块状碳酸钙固体;E为 一个空的蒸馏烧瓶;F是用于鼓入空气的双连打气球.