题目内容
已知在25℃时Ksp[Mg﹙OH﹚2]=3.2×10-11,假设饱和Mg﹙OH﹚2溶液的浓度为1g/mL,试求Mg﹙OH﹚2的溶解度为 .
考点:难溶电解质的溶解平衡及沉淀转化的本质
专题:
分析:根据溶度积计算c([Mg﹙OH﹚2),可计算100mL溶液中氢氧化镁的质量,进而计算溶解度.
解答:
解:设饱和溶液Mg﹙OH﹚2的物质的量浓度为c,则c(Mg2+)×c2(OH-)=4c3=3.2×10-11,c=2×10-4mol/L,
假设饱和Mg﹙OH﹚2溶液的浓度为1g/mL,则100mL溶液的质量为100g,含有溶质的质量为2×10-4mol/L×0.1L×58g/mol=1.16×10-3g.
故答案为:1.16×10-3g.
假设饱和Mg﹙OH﹚2溶液的浓度为1g/mL,则100mL溶液的质量为100g,含有溶质的质量为2×10-4mol/L×0.1L×58g/mol=1.16×10-3g.
故答案为:1.16×10-3g.
点评:本题考查物质的量的计算,侧重于饱和溶液和难溶电解质的理解,难度不大,注意把握相关计算公式.

练习册系列答案
 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案
相关题目
下列说法中(NA代表阿伏加德罗常数的值),不正确的是( )
| A、标准状况下,2.24LCO和CO2混合气体中含有的碳原子数目为0.1NA |
| B、常温下,2.3g Na完全与O2反应失去的电子数为0.1NA |
| C、100mL 18.4mol?L-1的硫酸与足量铜反应,生成二氧化硫的分子数小于0.92 NA |
| D、在密闭容器中加入1.5mol H2和0.5molN2,充分反应后可得到NH3分子数为NA |
某一定量的气态烷烃在氧气中完全燃烧生成a mol二氧化碳和b mol水,则下列说法正确的是( )
| A、该烷烃的物质的量为(b-a)mol |
| B、该烷烃的物质的量为a mol |
| C、该烷烃的物质的量为(b-a)/2 mol |
| D、不能求出该烷烃的物质的量 |
A、B、C为三种短周期元素,A、B在同一周期,A、C的最低价离子分别为A2-、C-,离子半径A2-大于C-,B2+和C-具有相同的电子层结构.下列判断正确的是( )
| A、原子序数由大到小的顺序是C>A>B |
| B、原子半径由大到小的顺序是r(B)>r(A)>r(C) |
| C、离子半径由大到小的顺序是r(C-)>r(B2+)>r(A2-) |
| D、原子最外层电子数由多到少的顺序是B>A>C |

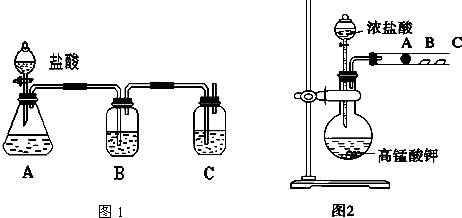
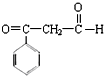 是一种重要的化工原料.A、B、C、D、E之间的转化关系如图:
是一种重要的化工原料.A、B、C、D、E之间的转化关系如图: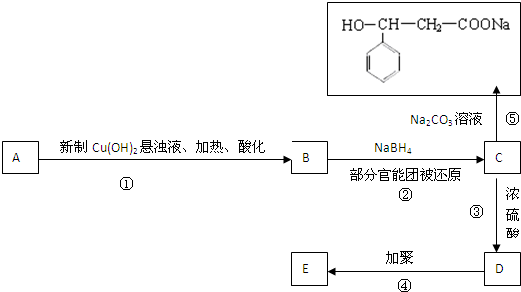
 某兴趣小组同学进行乙醛的银镜反应实验的操作步骤如下:
某兴趣小组同学进行乙醛的银镜反应实验的操作步骤如下: