题目内容
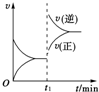 如图为某可逆反应的速率与时间的关系示意图,在t1时刻改变的条件为升温或增大压强,则该可逆反应可以是(提示:即升温或增大压强时均能符合如右图所示的速率与时间图象)( )
如图为某可逆反应的速率与时间的关系示意图,在t1时刻改变的条件为升温或增大压强,则该可逆反应可以是(提示:即升温或增大压强时均能符合如右图所示的速率与时间图象)( )| A、4NH3(g)+5O2(g)═4NO(g)+6H2O(g)△H<0 |
| B、2SO2(g)+O2(g)═2SO3(g)△H<0 |
| C、H2(g)+I2(g)═2HI(g)△H>0 |
| D、C(s)+H2O(g)═CO(g)+H2(g)△H>0 |
考点:化学平衡的影响因素
专题:化学平衡专题
分析:由图象可知,在t1时刻升高温度或增大压强,正逆反应速率都增大,且逆反应速率大于正反应速率,说明平衡向逆反应方向移动,结合温度、压强对平衡移动的影响解答该题.
解答:
解:在t1时刻升高温度或增大压强,正逆反应速率都增大,且逆反应速率大于正反应速率,说明平衡向逆反应方向移动,
如是升高温度,正反应应为放热反应,
如是增大压强,则反应物气体的计量数之和小于生成物气体的计量数之和,
只有A符合,
故选A.
如是升高温度,正反应应为放热反应,
如是增大压强,则反应物气体的计量数之和小于生成物气体的计量数之和,
只有A符合,
故选A.
点评:本题考查化学平衡图象问题,题目难度中等,根据图象判断平衡移动的方向,结合温度、压强对平衡移动的影响是解答该题的关键,学习中注意相关知识的积累.

练习册系列答案
 活力课时同步练习册系列答案
活力课时同步练习册系列答案 学业测评一课一测系列答案
学业测评一课一测系列答案
相关题目
下列有关化学用语表达正确的是( )
| A、二氧化硅的分子式:SiO2 |
B、H2O2的电子式: |
C、乙酸分子的球棍模型: |
D、离子结构示意图  可以表示35Cl-,也可以表示37Cl- 可以表示35Cl-,也可以表示37Cl- |
有一在空气中暴露过的KOH固体,经分析知含水7.12%,K2CO32.88%,KOH 90%,若将此样品1g加入到46.00mL 1mol/L盐酸中,过量的酸再用1.07mol/LKOH溶液恰好中和,蒸发中和后的溶液可得固体( )g.
| A、6.07 | B、2.62 |
| C、4.54 | D、3.43 |
某无色溶液,其中有可能存在的离子如下:Na+、Ag+、Ba2+、Al3+、AlO2-、S2-、CO32-、SO32-、SO42-.现取该溶液进行有关实验,实验结果如图所示:
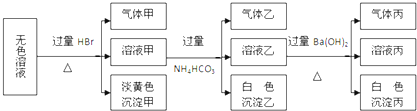
下列说法正确的是( )

下列说法正确的是( )
| A、沉淀甲可能是AgBr |
| B、沉淀丙一定是BaCO3 |
| C、气体甲的成份只有4种可能 |
| D、肯定存在的离子有AlO2-、S2-、SO32-、Na+ |
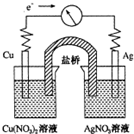 将反应Cu(s)+2Ag+(aq)═Cu2+(aq)+2Ag(s)设计成如图所示的原电池,下列叙述正确的是( )
将反应Cu(s)+2Ag+(aq)═Cu2+(aq)+2Ag(s)设计成如图所示的原电池,下列叙述正确的是( )| A、KNO3盐桥中的K+移向Cu(NO3)2溶液 |
| B、Ag作负极,Cu作正极 |
| C、工作一段时间后,Cu(NO3)2溶液中c(Cu2+)增大 |
| D、取出盐桥后,电流计的指针依然发生偏转 |
石油是重要的能源和化工原料,我国南海因为富含石油资源而被菲律宾等邻国觊觎.下列燃料不是从石油中分离出来的是( )
| A、煤油 | B、柴油 | C、酒精 | D、汽油 |
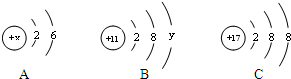 A、B、C三种元素的粒子结构示意图如图所示
A、B、C三种元素的粒子结构示意图如图所示 某溶液中可能含有的离子如下表:
某溶液中可能含有的离子如下表: