题目内容
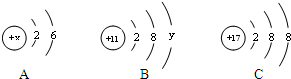 A、B、C三种元素的粒子结构示意图如图所示
A、B、C三种元素的粒子结构示意图如图所示(1)当A、B为原子时,x=
(2)C表示的粒子符号是Cl-,属于
考点:原子结构与元素的性质
专题:原子组成与结构专题
分析:(1)原子的核电荷数=核外电子总数,据此进行解答;
(2)C为氯离子,属于阴离子;氯原子的核电荷数=核外电子总数;氯元素与钠元素形成的氯化钠为离子化合物.
(2)C为氯离子,属于阴离子;氯原子的核电荷数=核外电子总数;氯元素与钠元素形成的氯化钠为离子化合物.
解答:
解:(1)当A、B为原子时,原子的原子序数=核电荷数=核外电子总数,所以x=2+6=8;2+8+y=11,则y=1,
故答案为:8;1;
(2)C为氯离子,为带有1个负电荷的阴离子;氯原子的最外层电子数为7;氯元素与钠元素形成的化合物为NaCl,属于离子化合物,由钠离子和氯离子构成,
故答案为:阴;7;离子.
故答案为:8;1;
(2)C为氯离子,为带有1个负电荷的阴离子;氯原子的最外层电子数为7;氯元素与钠元素形成的化合物为NaCl,属于离子化合物,由钠离子和氯离子构成,
故答案为:阴;7;离子.
点评:本题考查了原子结构与元素的性质,题目难度不大,试题侧重基础知识的考查,明确常见元素的原子结构与元素的性质即可解答,试题培养了学生灵活应用基础知识解决实际问题的能力.

练习册系列答案
 每课必练系列答案
每课必练系列答案 巧学巧练系列答案
巧学巧练系列答案
相关题目
2.0mol PCl3和1.0mol Cl2充入体积不变的密闭容器中,在一定条件下发生下述反应:PCl3(g)+Cl2(g)?PCl5(g) 达平衡时PCl5为0.40mol,如果此时再加入2.0mol PCl3和1.0mol Cl2,在相同温度下再达平衡时PCl5的物质的量是( )
| A、小于0.40 mol |
| B、大于0.80 mol |
| C、等于0.80 mol |
| D、大于0.40 mol,小于0.80 mol |
下列化学用语正确的是( )
| A、H2O的结构式:H-O-H |
| B、乙醇的结构简式:C2H6O |
C、H2O2的电子式: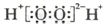 |
D、14C的原子结构示意图: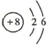 |
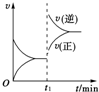 如图为某可逆反应的速率与时间的关系示意图,在t1时刻改变的条件为升温或增大压强,则该可逆反应可以是(提示:即升温或增大压强时均能符合如右图所示的速率与时间图象)( )
如图为某可逆反应的速率与时间的关系示意图,在t1时刻改变的条件为升温或增大压强,则该可逆反应可以是(提示:即升温或增大压强时均能符合如右图所示的速率与时间图象)( )| A、4NH3(g)+5O2(g)═4NO(g)+6H2O(g)△H<0 |
| B、2SO2(g)+O2(g)═2SO3(g)△H<0 |
| C、H2(g)+I2(g)═2HI(g)△H>0 |
| D、C(s)+H2O(g)═CO(g)+H2(g)△H>0 |