题目内容
16.图中A~I均为有机化合物,根据图中的信息,回答下列问题.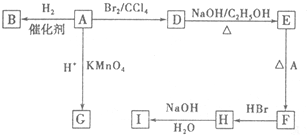
已知烯烃在强氧化剂酸性高锰酸钾作用下双键断裂,R为烃基
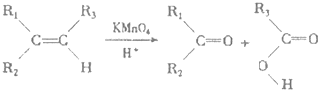
(1)0.2mol某环烃A在氧气中完全燃烧后,生成CO2 1.2mol和H2O 1.0mol,烃A的分子式为C6H10.B的一氯代物仅有一种,B的结构简式为
 .
.(2)M是B的一种同分异构体,M能使溴的四氯化碳溶液褪色,分子中所有的碳原子一定在同一平面内,则M的结构简式为(CH3)2C=C(CH3)2 .
(3)由A生成D的反应类型是加成反应,由D生成E的反应类型是消去反应.
(4)G的结构简式为HOOC(CH2)4COOH.
(5)分子中含有两个碳碳双键,且两个双键之间有一个碳碳单键的烯烃与单烯烃可发生如下反应:
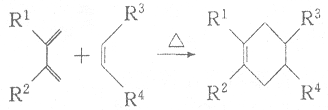
则由E和A反应生成F的化学方程式为
 .
.(6)H中含有的官能团的名称溴原子,I中含有的官能团的结构简式-OH.
(7)已知X、Y、Z是烃A的同分异构体
①X分子结构中无支链或侧链,它与Br2按物质的量1:1加成后的产物只有两种,X的系统命名是2,4-己二烯.
②Y分子中至少有4个碳原子在同一直线上,则符合该条件的Y的结构有3种.
③Z与等物质的量的氯气加成后的一种产物中,所有碳原子一定在同一平面,写出链烃Z生成该产物的化学方程式:CH2=C(CH3)C(CH3)=CH2+Cl2→ClCH2C(CH3)=C(CH3)CH2Cl.
(8)W比烃A相对分子质量小14,核磁共振氢谱显示它的分子中只有一组峰.则W的结构简式为
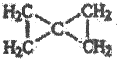 .
.
分析 环烃A中碳原子个数=$\frac{1.2mol}{0.2mol}$=6,氢原子个数=$\frac{1.0mol×2}{0.2mol}$=10,所以A的分子式为C6H10,A能和氢气发生加成反应生成B,说明A中含有碳碳双键,B的一氯代物仅有一种,说明环烷烃B没有支链,所以A为 ,则B为
,则B为 ,A和溴发生加成反应生成D为
,A和溴发生加成反应生成D为 ,D和氢氧化钠的醇溶液发生消去反应生成E,E能和A发生反应生成F,结合题给信息知,E的结构简式为:
,D和氢氧化钠的醇溶液发生消去反应生成E,E能和A发生反应生成F,结合题给信息知,E的结构简式为: ,F的结构简式为:
,F的结构简式为: ,F和HBr发生加成反应生成H,则H的结构简式为:
,F和HBr发生加成反应生成H,则H的结构简式为: ,H和氢氧化钠的水溶液发生取代反应生成I,I的结构简式为:
,H和氢氧化钠的水溶液发生取代反应生成I,I的结构简式为: ,A被酸性高锰酸钾氧化生成G,碳碳双键能被酸性高锰酸钾氧化生成羧酸,G的结构简式为HOOC(CH2)4COOH.
,A被酸性高锰酸钾氧化生成G,碳碳双键能被酸性高锰酸钾氧化生成羧酸,G的结构简式为HOOC(CH2)4COOH.
解答 解:环烃A中碳原子个数=$\frac{1.2mol}{0.2mol}$=6,氢原子个数=$\frac{1.0mol×2}{0.2mol}$=10,所以A的分子式为C6H10,A能和氢气发生加成反应生成B,说明A中含有碳碳双键,B的一氯代物仅有一种,说明环烷烃B没有支链,所以A为 ,则B为
,则B为 ,A和溴发生加成反应生成D为
,A和溴发生加成反应生成D为 ,D和氢氧化钠的醇溶液发生消去反应生成E,E能和A发生反应生成F,结合题给信息知,E的结构简式为:
,D和氢氧化钠的醇溶液发生消去反应生成E,E能和A发生反应生成F,结合题给信息知,E的结构简式为: ,F的结构简式为:
,F的结构简式为: ,F和HBr发生加成反应生成H,则H的结构简式为:
,F和HBr发生加成反应生成H,则H的结构简式为: ,H和氢氧化钠的水溶液发生取代反应生成I,I的结构简式为:
,H和氢氧化钠的水溶液发生取代反应生成I,I的结构简式为: ,A被酸性高锰酸钾氧化生成G,碳碳双键能被酸性高锰酸钾氧化生成羧酸,G的结构简式为HOOC(CH2)4COOH.
,A被酸性高锰酸钾氧化生成G,碳碳双键能被酸性高锰酸钾氧化生成羧酸,G的结构简式为HOOC(CH2)4COOH.
(1)由上述分析可知,A的分子式为C6H10,B的结构简式为 ,故答案为:C6H10;
,故答案为:C6H10; ;
;
(2)B的结构简式为 ,M是B的一种同分异构体,M能使溴的四氯化碳溶液褪色,说明含有碳碳双键,分子中所有的碳原子共平面,说明具有乙烯的结构特点,则M的结构简式为(CH3)2C=C(CH3)2 ,故答案为:(CH3)2C=C(CH3)2 ;
,M是B的一种同分异构体,M能使溴的四氯化碳溶液褪色,说明含有碳碳双键,分子中所有的碳原子共平面,说明具有乙烯的结构特点,则M的结构简式为(CH3)2C=C(CH3)2 ,故答案为:(CH3)2C=C(CH3)2 ;
(3)由A生成D的反应类型:加成反应,由D生成E的反应类型:消去反应,故答案为:加成反应;消去反应;
(4)G的结构简式为:HOOC(CH2)4COOH,故答案为:HOOC(CH2)4COOH;
(5)由信息可知,E和A发生加成反应生成F,该反应方程式为: ,
,
故答案为: .
.
(6)H为 ,含有的官能团为溴原子,I为
,含有的官能团为溴原子,I为 ,含有的官能团的结构简式 为-OH,故答案为:溴原子;-OH;
,含有的官能团的结构简式 为-OH,故答案为:溴原子;-OH;
(7)已知X、Y、Z是烃A( )的同分异构体:
)的同分异构体:
①X分子结构中无支链或侧链,它与Br2按物质的量1:1加成后的产物只有两种,则X为CH3CH=CHCH=CHCH3,名称为2,4-己二烯,故答案为:2,4-己二烯;
②Y分子中至少有4个碳原子在同一直线上,则含有碳碳双键,可能的结构简式有:CH3C≡CCH2CH2CH3,CH3C≡CC(CH3)2,CH3CH2C≡CCH2CH3,故答案为:3;
③Z与等物质的量的氯气加成后的一种产物中,所有碳原子一定在同一平面,则Z为CH2=C(CH3)C(CH3)=CH2,链烃Z生成该产物的化学方程式:CH2=C(CH3)C(CH3)=CH2+Cl2→ClCH2C(CH3)=C(CH3)CH2Cl,
故答案为:CH2=C(CH3)C(CH3)=CH2+Cl2→ClCH2C(CH3)=C(CH3)CH2Cl;
(8)W比烃A( )相对分子质量小14,W分子式为C5H8,核磁共振氢谱显示它的分子中只有一组峰.则W的结构简式为
)相对分子质量小14,W分子式为C5H8,核磁共振氢谱显示它的分子中只有一组峰.则W的结构简式为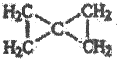 ,故答案为:
,故答案为: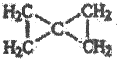 .
.
点评 本题考查有机物的推断,关键是确定A的结构简式,结合反应信息与反应条件进行推断,需要学生熟练掌握官能团的性质与转化,较好的考查学生自学能力与迁移运用能力,难度中等,为易错点.

| A. | NO | B. | CO | C. | NO2 | D. | O2 |
| A. | 标准状况下,2.24L苯含有的分子数为0.1NA | |
| B. | 常温常压下,18g H2O含有10nA个电子 | |
| C. | 1L1mol•L-1的NH4Cl溶液中有nA个NH4+ | |
| D. | 一定条件下,向密闭容器中投入3mol H2和1mol N2充分反应后可得到NH3分子数为2NA |
| A. | C2H6O | B. | C4H9Cl | C. | C3H8 | D. | C7H8 |
| A. | 0.75 mol | B. | 1.5 mol | C. | 1.0 mol | D. | 0.67 mol |
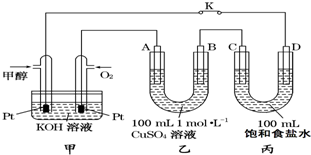 如图是甲醇(CH3OH)燃料电池工作的示意图,其中A、B、D均为石墨电极,C为铜电极.工作一段时间后,断开K,此时A、B两极上产生的气体体积相同.
如图是甲醇(CH3OH)燃料电池工作的示意图,其中A、B、D均为石墨电极,C为铜电极.工作一段时间后,断开K,此时A、B两极上产生的气体体积相同.