题目内容
下列现象或事实不能用同一原理解释的是( )
| A、浓硝酸和氯水用棕色试剂瓶保存 |
| B、硫化钠和亚硫酸钠固体长期暴露在空气中变质 |
| C、常温下铁和铂都不溶于浓硝酸 |
| D、SO2和Na2SO3溶液都能使氯水褪色 |
考点:硝酸的化学性质,氯气的化学性质,二氧化硫的化学性质,含硫物质的性质及综合应用
专题:元素及其化合物
分析:A.浓硝酸见光易分解;氯水见光会分解;
B.硫化钠具有还原性,易被空气中的氧气氧化而变质;亚硫酸钠具有还原性,易被空气中的氧气氧化而变质;
C.常温下铁遇浓硝酸,发生钝化;铂的活泼性较弱,与浓硝酸不反应;
D.SO2具有还原性,能与氯水发生氧化还原反应使氯水褪色;Na2SO3具有还原性,能与氯水发生氧化还原反应使氯水褪色.
B.硫化钠具有还原性,易被空气中的氧气氧化而变质;亚硫酸钠具有还原性,易被空气中的氧气氧化而变质;
C.常温下铁遇浓硝酸,发生钝化;铂的活泼性较弱,与浓硝酸不反应;
D.SO2具有还原性,能与氯水发生氧化还原反应使氯水褪色;Na2SO3具有还原性,能与氯水发生氧化还原反应使氯水褪色.
解答:
解:A.浓硝酸见光易分解,须存放在棕色瓶中;氯水见光会分解,应盛放在棕色瓶中,能用同一原理解释,故A不选;
B.硫化钠具有还原性,易被空气中的氧气氧化而变质;亚硫酸钠具有还原性,易被空气中的氧气氧化而变质,能用同一原理解释,故B不选;
C.常温下铁遇浓硝酸,发生钝化;铂的活泼性较弱,与浓硝酸不反应,不能用同一原理解释,故C可选;
D.SO2具有还原性,能与氯水发生氧化还原反应使氯水褪色;Na2SO3具有还原性,能与氯水发生氧化还原反应使氯水褪色;能用同一原理解释,故D不选;
故选C.
B.硫化钠具有还原性,易被空气中的氧气氧化而变质;亚硫酸钠具有还原性,易被空气中的氧气氧化而变质,能用同一原理解释,故B不选;
C.常温下铁遇浓硝酸,发生钝化;铂的活泼性较弱,与浓硝酸不反应,不能用同一原理解释,故C可选;
D.SO2具有还原性,能与氯水发生氧化还原反应使氯水褪色;Na2SO3具有还原性,能与氯水发生氧化还原反应使氯水褪色;能用同一原理解释,故D不选;
故选C.
点评:本题考查物质的保存、金属的钝化、硫的化合物的性质等,难度中等.要注意基础知识的积累.

练习册系列答案
相关题目
关于CaCO3沉淀的溶解平衡说法正确的是( )
| A、CaCO3沉淀生成和沉淀溶解不断进行,但速率相等 |
| B、CaCO3难溶于水,溶液中没有Ca2+和CO32- |
| C、升高温度,CaCO3沉淀的溶解度无影响 |
| D、向CaCO3沉淀中加入Na2CO3固体,CaCO3沉淀的溶解度不变 |
在元素周期表中碳元素的信息如图所示,下列说法正确的是( )


| A、碳原子中的质子数为6 |
| B、碳的相对原子质量是12.01g |
| C、碳属于金属元素 |
| D、碳的氧化物只有一种 |
25°C时,KSPMg(OH)2=5.61×10-12,KSP MgF2=7.42×10-11下列说法正确的是( )
| A、25°C时,饱和Mg(OH)2溶液与饱和MgF2溶液相比,前者的C(Mg)2+大 |
| B、25°C时,固体在20ml0.01 mol?L-1氨水中的比20mL0.01 mol?L-1NH4Cl溶液中的KSP小 |
| C、25°C时,在Mg(OH)2的悬浊液加入少量的NH4Cl固体,C(Mg2+)增大 |
| D、25°C时,在Mg(OH)2的悬浊液加入NaF溶液后,Mg(OH)2不可能转化成为MgF2 |
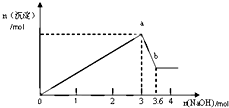 有一无色透明溶液,可能含Al3+、Fe3+、Mg2+、Na+、CO32-、Cl-、NO3-等离子中的若干种.现做如下实验:
有一无色透明溶液,可能含Al3+、Fe3+、Mg2+、Na+、CO32-、Cl-、NO3-等离子中的若干种.现做如下实验: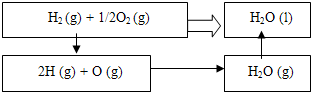


 在一定条件下可水解为
在一定条件下可水解为 和R2-NH2.H在一定条件下水解的产物之一为氨基酸M,则由M形成二肽的化学方程式为
和R2-NH2.H在一定条件下水解的产物之一为氨基酸M,则由M形成二肽的化学方程式为