题目内容
15.下列离子方程式正确的是( )| A. | 少量SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-═CaSO3↓+2HClO | |
| B. | 氯化铁溶液和铜反应:Fe3++Cu═Fe2++Cu2+ | |
| C. | 石灰水与碳酸氢钠溶液混合:Ca2++CO32-═CaCO3↓ | |
| D. | 硫酸氢钠溶液中加入氢氧化钡溶液至中性:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O |
分析 A.次氯酸具有强氧化性,与亚硫酸钙反应生成硫酸钙;
B.离子方程式两边正电荷不相等,违反了电荷守恒;
C.碳酸氢根离子不能拆开,反应生成碳酸钙沉淀和水;
D.溶液为中性时,硫酸氢钠与氢氧化钡按照物质的量2:1反应.
解答 解:A.次氯酸能够氧化亚硫酸钙,正确的离子方程式为:Ca2++3ClO-+H2O+SO2═CaSO4↓+2HClO+Cl-,故A错误;
B.氯化铁溶液和铜反应生成氯化亚铁和氯化铜,正确的离子方程式为:2Fe3++Cu═2Fe2++Cu2+,故B错误;
C.碳酸氢根离子不能拆开,若氢氧化钙过量时正确的离子方程式为:Ca2++HCO3-+OH-=CaCO3↓+H2O,故C错误;
D.硫酸氢钠溶液中加入氢氧化钡溶液至中性,氢离子与氢氧根离子的物质的量相等,反应的离子方程式为:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O,故D正确;
故选D.
点评 本题考查了离子方程式的书写判断,为高考的高频题,属于中等难度的试题,注意掌握离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
5.下列实验现象描述不正确的是( )
| 选项 | 实验 | 现象 |
| A | 加热放在坩埚中的小块钠 | 钠先熔化成光亮的小球,燃烧时,火焰为黄色,燃烧后,生成淡黄色固体 |
| B | 在酒精灯上加热铝箔 | 铝箔熔化,失去光泽,熔化的铝并不滴落, 好像有一层膜兜着 |
| C | 点燃的镁条伸入盛有O2的集气瓶(底部铺有少量细砂)中 | 镁条继续燃烧,发出耀眼白光放出大量热量,生成白色固体 |
| D | 在空气中久置的铝条放入NaOH溶液中 | 立刻产生大量无色气泡,铝条逐渐变细, 铝条逐渐发热 |
| A. | A | B. | B | C. | C | D. | D |
6.下列对CO2的说法正确的是( )
| A. | 由非极性键构成的非极性分子 | B. | 中心原子的杂化方式是sp2 | ||
| C. | 该分子的空间构型是平面三角形 | D. | 1mol该分子有2mol σ键 |
10.“混盐”是指一种金属离子与多种酸根阴离子构成的盐,如氯化硝酸钙[Ca(NO3)Cl]就是一种混盐.“复盐”是指含多种简单阳离子和一种酸根阴离子构成的盐,如:KAl(SO4)2.下列化合物中属于“混盐”的是( )
| A. | BiONO3 | B. | (NH4)2Fe(SO4)2 | C. | Ca(ClO)Cl | D. | K3Fe(CN)6 |
20.CO和NO都是汽车尾气中的有害气体,它们在催化转化器中能反应生成N2和CO2,对此反应,下列说法中错误的是( )
| A. | 改变压强不可以改变反应速率 | |
| B. | 使用催化剂能同时增大正、逆反应的速率 | |
| C. | 增大压强能增大反应速率 | |
| D. | 升高温度能增大反应速率 |
7.如图是一种有机物的比例模型,该模型代表的有机物可能是( )


| A. | 饱和一元醇 | B. | 羟基酸 | C. | 羧酸 | D. | 饱和一元醛 |
4.用NA表示阿伏伽德罗常数,下列叙述正确的是( )
| A. | 标准状况下,5.6LH2O含有的分子数为0.25NA | |
| B. | 常温常压下,1.06gNa2CO3含有Na+离子数为0.02NA | |
| C. | 通常情况下,NA个CO2分子占有的体积为22.4L | |
| D. | 物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl-个数为NA |
5.下列说法正确的是( )
| A. | 用乙醇作萃取剂可以将碘从碘水中萃取出来 | |
| B. | 酒精用来杀菌消毒,利用了乙醇的氧化性 | |
| C. | 石油的裂化的主要目的是提高汽油的质量和产量 | |
| D. | 苯环上的碳碳键是一种介于单键和双键的独特的键,苯既不能发生取代反应也不能发生加成反应 |
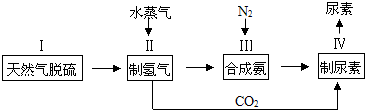
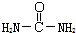 ,请写出尿素的同分异构体中含有离子键的化学式NH4OCN.
,请写出尿素的同分异构体中含有离子键的化学式NH4OCN.