题目内容
5.下列说法正确的是( )| A. | 用乙醇作萃取剂可以将碘从碘水中萃取出来 | |
| B. | 酒精用来杀菌消毒,利用了乙醇的氧化性 | |
| C. | 石油的裂化的主要目的是提高汽油的质量和产量 | |
| D. | 苯环上的碳碳键是一种介于单键和双键的独特的键,苯既不能发生取代反应也不能发生加成反应 |
分析 A.乙醇易溶于水,不能用作萃取剂;
B.乙醇无强氧化性;
C.石油裂化的目的是为了提高轻质液体燃料的产量,特别是提高汽油的产量;
D.苯可发生取代、加成反应.
解答 解:A.乙醇易溶于水,不能用作萃取剂,一般用苯、四氯化碳,故A错误;
B.乙醇无强氧化性,酒精能使蛋白质变性而杀菌消毒,故B错误;
C.石油裂化的目的是为了提高轻质液体燃料(汽油,煤油,柴油等)的产量,特别是提高汽油的产量,故C正确;
D.苯环上的碳碳键是一种介于单键和双键的独特的键,苯可发生取代、加成反应,故D错误.
故选C.
点评 本题考查较为综合,涉及物质的分离、提纯以及有机物的结构和性质,侧重于学生基础知识的考查,注意把握常见物质的性质以及分离实验方法的操作原理、步骤以及注意事项等,注意相关基础知识的学习,难度不大.

练习册系列答案
相关题目
15.下列离子方程式正确的是( )
| A. | 少量SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-═CaSO3↓+2HClO | |
| B. | 氯化铁溶液和铜反应:Fe3++Cu═Fe2++Cu2+ | |
| C. | 石灰水与碳酸氢钠溶液混合:Ca2++CO32-═CaCO3↓ | |
| D. | 硫酸氢钠溶液中加入氢氧化钡溶液至中性:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O |
13.已知25℃、101kPa条件下:
(1)4Al(s)+3O2(g)═2Al2O3(s)△H=-2 834.9kJ•mol-1
(2)4Al(s)+2O3(g)═2Al2O3(s)△H=-3 119.1kJ•mol-1
由此得出的正确结论是( )
(1)4Al(s)+3O2(g)═2Al2O3(s)△H=-2 834.9kJ•mol-1
(2)4Al(s)+2O3(g)═2Al2O3(s)△H=-3 119.1kJ•mol-1
由此得出的正确结论是( )
| A. | O2比O3稳定,由O2变O3为放热反应 | |
| B. | O3比O2稳定,由O2变O3为吸热反应 | |
| C. | 等质量的O2比O3能量低,由O2变O3为吸热反应 | |
| D. | 等质量的O2比O3能量高,由O2变O3为放热反应 |
20.某非金属元素R的氢化物及其氧化物、盐之间具有如下转化关系(部分产物省略):氢化物$\stackrel{氧气}{→}$B$\stackrel{Na_{2}O_{2}}{→}$ C,下列判断中正确的是( )
| A. | 若R是硫元素、则C是Na2SO3 | B. | 若R是硅元素、则C是Na2Si03 | ||
| C. | 若R是碳元素、则C是Na2CO3 | D. | 若R是氯元素、则C是NaCl |
10.将NO2装入带活塞的密闭容器中,当反应2NO2(g)?N2O4(g)达到平衡后,改变下列一个条件,其中叙述正确的是( )
| A. | 升高温度,气体颜色加深,则此反应为吸热反应 | |
| B. | 慢慢压缩气体体积,平衡向右移动,混合气体颜色变浅 | |
| C. | 慢慢压缩气体体积,若体积减小一半,压强增大,但小于原来的两倍 | |
| D. | 恒温恒容时,充入NO2气体,平衡向右移动,NO2的转化率增大,混合气体的颜色变浅 |
17.下列叙述正确的是( )
| A. | 1.00mol NH4Cl中含有6.02×1023个NH4Cl分子 | |
| B. | 1.00mol NH4Cl中,${NH}_{4}^{+}$的数目为6.02×1023 | |
| C. | 欲配制1.00L 1.00mol•L-1NH4CL的溶液,可将53.5gNH4Cl溶于1.00L水中 | |
| D. | 1.00L 1.00mol•L-1 NH4Cl溶液中含有6.02×1023个NH3分子 |
14.丙烯与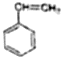 按1:1聚合所得的产物中,聚合物的结构简式可能有几种表现形式( )
按1:1聚合所得的产物中,聚合物的结构简式可能有几种表现形式( )
 按1:1聚合所得的产物中,聚合物的结构简式可能有几种表现形式( )
按1:1聚合所得的产物中,聚合物的结构简式可能有几种表现形式( )| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
13.用NA表示阿伏加德罗常数的值.下列判断正确的是( )
| A. | 常温常压下,22.4L N2含有的分子数为NA | |
| B. | 1mol•L-1 Al2(SO4)3溶液中含SO42-数目为3NA | |
| C. | 常温常压下,46g NO2含有氧原子数为2NA | |
| D. | 1mol Fe在足量Cl2中燃烧,转移电子数为2NA |
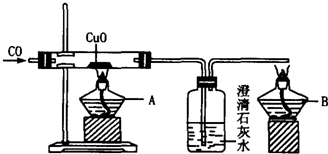
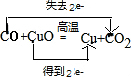 ,CuO、CO
,CuO、CO