题目内容
6.下列对CO2的说法正确的是( )| A. | 由非极性键构成的非极性分子 | B. | 中心原子的杂化方式是sp2 | ||
| C. | 该分子的空间构型是平面三角形 | D. | 1mol该分子有2mol σ键 |
分析 A.不同非金属原子间形成极性键,分子结构对称正负电荷中心重叠为非极性分子;
B.根据C原子的价层电子对数判断;
C.根据杂化类型判断;
D.二氧化碳的结构式为O=C=O,一个双键中含有1σ键和1个π键.
解答 解:A.CO2中存在C、O极性键,没有非极性键,CO2分子结构对称正负电荷中心重叠为非极性分子,故A错误;
B.CO2中C原子的价层电子对数为2,属于sp杂化,故B错误;
C.CO2中C原子的价层电子对数为2,属于sp杂化,分子的空间构型是直线形,故C错误;
D.二氧化碳的结构式为O=C=O,一个双键中含有1σ键和1个π键,则1mol该分子有2mol σ键,故D正确.
故选D.
点评 本题考查了共价键、分子的极性判断、杂化理论的应用等,题目难度不大,侧重于考查学生对基础知识的综合应用能力,注意把握杂化类型的判断方法.

练习册系列答案
 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案
相关题目
17.下列各组物质,按强电解质、弱电解质、非电解质、既不是电解质又不是非电解质的顺序排列的是( )
| A. | NaOH、NaCl、SO2、NaCl溶液 | B. | BaSO4、SO3、CuSO4晶体、Na2O2 | ||
| C. | NaCl、H2S、CO2、Cu | D. | SO3、AgCl、NH3、H2O、Ag |
14.下列关于金属钠的说法中,正确的是( )
| A. | 钠与氧气反应的产物与反应条件无关 | |
| B. | 钠在反应中易失电子,表现出还原性 | |
| C. | 钠在氯气中燃烧产生红色火焰 | |
| D. | 钠只有在加热条件下才能与氯气发生反应 |
1.下列分子中,空间构型是平面三角形的是( )
| A. | BeCl2 | B. | BF3 | C. | CCl4 | D. | H2O |
11.下列关于物质的分类中正确的是( )
| 纯净物 | 混合物 | 强电解质 | 弱电解质 | 非电解质 | |
| A | 盐酸 | 漂白粉 | 硫酸 | 醋酸 | 干冰 |
| B | 氢氧化钡 | 蔗糖溶液 | 氯化银 | 溴水 | 二氧化硫 |
| C | 胆矾 | 石灰水 | 氧化铝 | 水 | 氯气 |
| D | 小苏打 | 氢氧化 铁胶体 | 胆矾 | 次氯酸 | 酒精 |
| A. | A | B. | B | C. | C | D. | D |
18.下列金属冶炼的反应原理,错误的是( )
| A. | 2NaCl(熔融)$\frac{\underline{\;电解\;}}{\;}$ 2Na+Cl2↑ | B. | MgO+H2 $\frac{\underline{\;\;△\;\;}}{\;}$Mg+H2O | ||
| C. | Fe3O4+4CO$\frac{\underline{\;高温\;}}{\;}$ 3Fe+4CO2 | D. | 2HgO$\frac{\underline{\;\;△\;\;}}{\;}$2Hg+O2 |
15.下列离子方程式正确的是( )
| A. | 少量SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-═CaSO3↓+2HClO | |
| B. | 氯化铁溶液和铜反应:Fe3++Cu═Fe2++Cu2+ | |
| C. | 石灰水与碳酸氢钠溶液混合:Ca2++CO32-═CaCO3↓ | |
| D. | 硫酸氢钠溶液中加入氢氧化钡溶液至中性:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O |
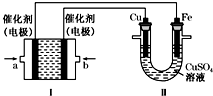 回答下列问题:
回答下列问题: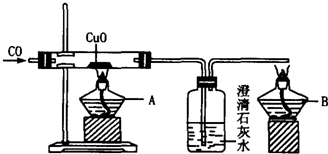
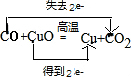 ,CuO、CO
,CuO、CO