题目内容
在中学化学实验中可用于分离或提纯的方法很多,如蒸馏、结晶、过滤、盐析等,下列各组混合物的分离或提纯选用方法最合适的是( )
| A、除去AgI胶体中混有的I-离子--过滤、洗涤、干燥 |
| B、除去苯中含有的少量苯酚--加入NaOH溶液、分液 |
| C、分离CuSO4?5H2O和BaSO4的混合物--溶解、过滤 |
| D、除去乙酸乙酯中混有的乙酸杂质--加入NaOH溶液、分液 |
考点:化学实验方案的评价
专题:实验评价题
分析:A.除去AgI胶体中混有的I-离子可用渗析的方法;
B.苯酚可与氢氧化钠溶液反应;
C.过滤后还需要结晶操作,以生成CuSO4?5H2O;
D.乙酸乙酯和乙酸都与氢氧化钠反应.
B.苯酚可与氢氧化钠溶液反应;
C.过滤后还需要结晶操作,以生成CuSO4?5H2O;
D.乙酸乙酯和乙酸都与氢氧化钠反应.
解答:
解:A.胶体粒子和离子都可透过滤纸,不能用过滤的方法分离,但胶体粒子不能透过半透膜,可用渗析的方法分离,故A错误;
B.苯酚可与氢氧化钠溶液反应,而苯不反应,可用分液的方法分离,故B正确;
C.过滤后不能得到硫酸铜晶体,还需要结晶操作,以生成CuSO4?5H2O,故C错误;
D.乙酸乙酯和乙酸都与氢氧化钠反应,应用饱和碳酸钠溶液分离,故D错误.
故选B.
B.苯酚可与氢氧化钠溶液反应,而苯不反应,可用分液的方法分离,故B正确;
C.过滤后不能得到硫酸铜晶体,还需要结晶操作,以生成CuSO4?5H2O,故C错误;
D.乙酸乙酯和乙酸都与氢氧化钠反应,应用饱和碳酸钠溶液分离,故D错误.
故选B.
点评:本题考查物质的分离方案的设计,为高频考点,侧重于学生的分析能力和实验能力的考查,题目难度不大,分离物质,应根据物质性质的异同,注意不能影响被提纯物质的性质.

练习册系列答案
相关题目
从理论上分析,碳原子数小于10的烷烃分子中,其一卤代物不存在同分异构体的烷烃分子共有的种数是( )
| A、3 | B、4 | C、5 | D、6 |
下列各装置中,烧杯中盛有海水,能够形成原电池并且铁为正极的是( )
A、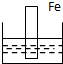 |
B、 |
C、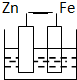 |
D、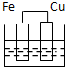 |
下列溶液中,阴离子浓度最大的是( )
| A、0.5mol/L HCl溶液50mL |
| B、0.6mol/L Al2(SO4)3溶液40mL |
| C、0.7mol/L NaCl溶液70mL |
| D、0.8mol/L Na2CO3溶液60mL |
下列分散系中最稳定的是( )
| A、豆浆 |
| B、FeCl3溶液 |
| C、泥水 |
| D、Fe(OH)3胶体 |
部分氧化的Fe-Cu合金样品(氧化产物为Fe2O3、CuO)共2.88g,经如下处理:下列说法正确的是( )


| A、滤液A中的阳离子为Fe2+、Fe3+、H+ |
| B、V=224 |
| C、样品中CuO的质量为2.0g |
| D、样品中Fe元素的质量为1.07g |
关于下列各装置图的叙述中,不正确的是( )


| A、若采用装置①精炼铜,则d极为粗铜,c极为纯铜,电解质溶液为CuSO4溶液 |
| B、装置②是原电池,能将化学能转化为电能,锌电极发生氧化反应 |
| C、装置③中X若为四氯化碳,可用于吸收氨气或氯化氢,并防止倒吸 |
| D、装置④可用于干燥、收集氨气,并吸收多余的氨气 |
将过量Cl2通入NaBr和NaI的混合液中,然后把混合溶液蒸干,再将剩余残渣灼烧,最后留下的物质( )
| A、NaBr,NaI |
| B、NaCl,NaBr |
| C、NaCl |
| D、NaCl,I2 |