题目内容
(1)离子检验时要注意排除离子的干扰,请思考:欲验证某溶液中是否含有SO42-离子,所加试剂均为足量,则加入试剂的先后顺序为(写化学式) 、 .
(2)欲验证某溶液中是否含有Cl-,所加试剂为(写化学式) 、 .
(3)使用容量瓶必须先进行 ,具体操作: .
(2)欲验证某溶液中是否含有Cl-,所加试剂为(写化学式)
(3)使用容量瓶必须先进行
考点:物质的检验和鉴别的基本方法选择及应用,常见阴离子的检验
专题:化学实验基本操作
分析:(1)在检验SO42-时,加入氯化钡之前要先加盐酸以排除CO32-离子的干扰;
(2)欲验证某溶液中是否含有Cl-,可加入硝酸银、硝酸,生成的氯化银不溶于硝酸;
(3)容量瓶在使用前必须检查是否漏水.
(2)欲验证某溶液中是否含有Cl-,可加入硝酸银、硝酸,生成的氯化银不溶于硝酸;
(3)容量瓶在使用前必须检查是否漏水.
解答:
解:(1)检验 SO42- 时要避免 SO32- 的影响,就不要加入稀硝酸,因为稀硝酸能把SO32- 氧化为SO42-,从而干扰SO42- 的检验;要先加入过量稀盐酸,以除去 SO32-、CO32- 等离子的影响,同时,当加入稀盐酸时没有沉淀,可排除Ag+的影响.当然,若溶液中不含SO32-离子,则加入稀硝酸也可.检验SO42-可用BaCl2溶液,看有没有白色沉淀产生.综上分析可知,检验某溶液中是否含有SO42-的操作方法是:首先在试液中加入盐酸酸化,再加入BaCl2溶液,若有BaSO4白色沉淀产生,则证明有SO42-.
故答案为:HCl;BaCl2;
(2)因为AgCl不溶于水,不溶于稀硝酸,因此,在检验Cl-时,要加入硝酸银溶液,但是CO32- 等离子也能与硝酸银生成沉淀,但能溶于稀硝酸,因此,在加入硝酸银之前,一定要加入稀硝酸来除去CO32- 等离子.综上分析,检验某溶液中是否含有Cl-的操作方法是:在试液中加入硝酸酸化的硝酸银溶液,若有白色沉淀产生,则证明有Cl-.
故答案为:HNO3;AgNO3;
(3)容量瓶在使用前必须检查是否漏水,方法是向容量瓶中注入少量水,塞紧玻璃塞,用手指按住瓶塞,另一只手按住瓶底倒转容量瓶,一段时间后观察瓶塞处是否有液体渗出,若无液体渗出,将其放正,把玻璃塞旋转180°,再倒转观察,
故答案为:检漏;向容量瓶中注入少量水,塞紧玻璃塞,用手指按住瓶塞,另一只手按住瓶底倒转容量瓶,一段时间后观察瓶塞处是否有液体渗出,若无液体渗出,将其放正,把玻璃塞旋转180°,再倒转观察.
故答案为:HCl;BaCl2;
(2)因为AgCl不溶于水,不溶于稀硝酸,因此,在检验Cl-时,要加入硝酸银溶液,但是CO32- 等离子也能与硝酸银生成沉淀,但能溶于稀硝酸,因此,在加入硝酸银之前,一定要加入稀硝酸来除去CO32- 等离子.综上分析,检验某溶液中是否含有Cl-的操作方法是:在试液中加入硝酸酸化的硝酸银溶液,若有白色沉淀产生,则证明有Cl-.
故答案为:HNO3;AgNO3;
(3)容量瓶在使用前必须检查是否漏水,方法是向容量瓶中注入少量水,塞紧玻璃塞,用手指按住瓶塞,另一只手按住瓶底倒转容量瓶,一段时间后观察瓶塞处是否有液体渗出,若无液体渗出,将其放正,把玻璃塞旋转180°,再倒转观察,
故答案为:检漏;向容量瓶中注入少量水,塞紧玻璃塞,用手指按住瓶塞,另一只手按住瓶底倒转容量瓶,一段时间后观察瓶塞处是否有液体渗出,若无液体渗出,将其放正,把玻璃塞旋转180°,再倒转观察.
点评:本题综合考查离子的检验以及容量瓶的使用,为高频考点,侧重于学生的分析、实验能力的考查,注意把握离子的检验方法,难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列说法正确的是( )
| A、Zn2+的4s轨道和4p轨道可以形成sp3杂化轨道,那么[ZnCl4]的空间构型为正四面体形 |
| B、NaOH中既有离子键又有共价键和配位键 |
| C、电解饱和食盐水的实验中阳极产生NaOH |
| D、在[Cu(NH3)4]2+离子中,Cu2+提供孤对电子对,NH3提供空轨道 |
实验室制备氨气,检验是否收集满的正确方法是( )
| A、用手扇动收集的气体,有气味则已收集满 |
| B、将润湿的淀粉KI试纸接近瓶口,试纸变蓝则已收集满 |
| C、将润湿的红色石蕊试纸伸入瓶内,试纸变蓝则已收集满 |
| D、用玻璃棒一端蘸取浓盐酸,接近瓶口,产生大量白烟,证明已收集满 |
设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A、5.6 g铁分别与足量的盐酸、氯气反应,电子转移总数均为0.3NA |
| B、14g乙烯、丙烯的混合气体含有C-H数为2NA |
| C、标准状况下,4.48L重水(D2O)中含有的中子数为2NA |
| D、向FeI2溶液中通入适量Cl2,当有1 mol Fe2+被氧化时,共转移的电子的数目为NA |


 将1mol I2(g)和2mol H2置于2L密闭容器中,在一定温度下发生反应:I2(g)+H2 (g)?2HI(g);△H<0,并达平衡.HI的物质的量分数w(HI)随时间变化如图曲线(Ⅱ)所示:
将1mol I2(g)和2mol H2置于2L密闭容器中,在一定温度下发生反应:I2(g)+H2 (g)?2HI(g);△H<0,并达平衡.HI的物质的量分数w(HI)随时间变化如图曲线(Ⅱ)所示:
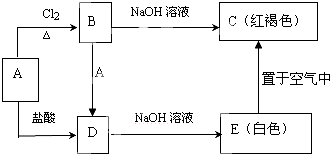 某金属A及其化合物之间有如下转化关系.
某金属A及其化合物之间有如下转化关系.