题目内容
下列说法正确的是( )
| A、Zn2+的4s轨道和4p轨道可以形成sp3杂化轨道,那么[ZnCl4]的空间构型为正四面体形 |
| B、NaOH中既有离子键又有共价键和配位键 |
| C、电解饱和食盐水的实验中阳极产生NaOH |
| D、在[Cu(NH3)4]2+离子中,Cu2+提供孤对电子对,NH3提供空轨道 |
考点:判断简单分子或离子的构型,配合物的成键情况
专题:化学键与晶体结构
分析:A、Zn2+的4s轨道和4p轨道可以形成sp3型杂化轨道,[ZnCl4]2-中的配位数是4,据此判断其空间结构;
B、氢氧化钠中存在离子键和共价键;
C、电解饱和食盐水,NaOH在阴极区域产生;
D.配合物中,配位体提供孤电子对,中心原子提供空轨道形成配位键.
B、氢氧化钠中存在离子键和共价键;
C、电解饱和食盐水,NaOH在阴极区域产生;
D.配合物中,配位体提供孤电子对,中心原子提供空轨道形成配位键.
解答:
解:A、此配离子的中心原子采取sp3杂化,配位数为4,故空间构型为正四面体型,故A正确;
B、氢氧化钠中钠离子和氢氧根离子之间存在离子键,氧原子和氢原子之间存在共价键,不含配位键,故B错误;
C、电解饱和食盐水,阴极生成NaOH和氢气,故C错误;
D.在[Cu(NH3)4]2+离子中,Cu2+提供空轨道,NH3提供孤电子对,故D错误;
故选A.
B、氢氧化钠中钠离子和氢氧根离子之间存在离子键,氧原子和氢原子之间存在共价键,不含配位键,故B错误;
C、电解饱和食盐水,阴极生成NaOH和氢气,故C错误;
D.在[Cu(NH3)4]2+离子中,Cu2+提供空轨道,NH3提供孤电子对,故D错误;
故选A.
点评:本题考查较为综合,涉及离子空间构型的判断、化学键的判断、配位键以及电解等知识,题目难度较大,注意把握电解原理.

练习册系列答案
 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案
相关题目
下列说法中错误的是( )
| A、1gO2与1gO3所含的原子数目相等 |
| B、不同分散系其对应分散质的微粒直径不同 |
| C、标况下1molCCl4所占体积约为22.4L |
| D、NaCl晶体和熔化的NaCl都属于电解质 |
表为元素周期表短周期的一部分,下列有关A、B、C、D四种元素的叙述正确的是( )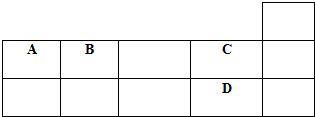

| A、原子半径的大小为A>B>C>D |
| B、D的氢化物在同族元素的氢化物中沸点最低 |
| C、生成氢化物的稳定性为A>B>C>D |
| D、A、B、C、D的单质常温下均不导电 |
下列各组反应,实质都是取代反应的是( )
| A、苯硝化,苯酚和溴水反应,皂化反应,油脂的硬化 |
| B、酯的水解,酯化反应,乙醇和氢卤酸反应,乙醇和浓硫酸加热至140℃时的反应 |
| C、淀粉在硫酸存在下制葡萄糖,醛的氧化或还原 |
| D、纤维素水解,浓硫酸和乙醇在170℃时的反应,蛋白质水解 |
在给定的四种溶液中,同时加入以下各种离子,可能在该溶液中大量共存的是( )
| A、pH为1的溶液:Ca2+、Na+、Mg2+、NO3- |
| B、滴加石蕊试液显红色的溶液:Fe3+、NH4+、Cl-、SCN- |
| C、与铝反应放出氢气的溶液:K+、HCO3-、Br-、Ba2+ |
| D、所含溶质为FeCl2的溶液:K+、SO42-、NO3-、H+ |
已知在标准状况下的四种气体 ①6.72L CH4;②3.01×1023个HCl分子;③13.6克H2S;④0.2molNH3该条件下体积最大和含氢原子数最多的依次是( )
| A、②和① | B、②和④ |
| C、①和④ | D、③和① |
下列离子方程式中书写正确的是( )
| A、NaHSO4在水溶液的电离方程式 NaHSO4?Na++H++SO42- |
| B、氯化铵在氘水中的水解离子方程式 NH4++D2O?NH3.HDO-+D+ |
| C、NaHS在水中的水解离子方程式 HS-+H2O?S2-+H3O+ |
| D、碳酸钙在水中的溶解平衡方程式 CaCO3=Ca2++CO32- |
 氧族元素的单质及其化合物对人类的生活、生产有着举足轻重的影响.
氧族元素的单质及其化合物对人类的生活、生产有着举足轻重的影响.